ความสำคัญของการดูแลรักษาก้อนที่ตับต้องแยกให้ได้ว่าเป็นเนื้องอกไม่ร้ายแรง (benign) หรือเป็นมะเร็ง (malignant) ซึ่งต้องอาศัยข้อมูลเพื่อช่วยในการวินิจฉัย ได้แก่ ประวัติการเจ็บป่วย เช่น การติดเชื้อไวรัสตับอักเสบบีหรือซี (chronic hepatitis B or C infection) ภาวะตับแข็ง, การตรวจร่างกาย,การตรวจทางห้องปฏิบัติการ เช่น การตรวจหน้าที่, การทำงานของตับ tumor marker (alpha-feto-protein, CEA, CA
19-9),ลักษณะที่เห็นจากการตรวจทางรังสีวิทยา เช่น เป็นซิสต์ หรือก้อนทึบ. อย่างไรก็ดี ในผู้ป่วยบางรายอาจต้องได้รับการตรวจเพิ่มเติม เช่น การเจาะชิ้นเนื้อตรวจ (liver mass biopsy) หรือการผ่าตัดตัดชิ้นเนื้อออกเพื่อให้ได้มาซึ่งการวินิจฉัยโรคและการรักษาไปพร้อมๆ กัน.
แนวทางในการวินิจฉัยโรคที่เป็นสาเหตุของก้อนที่ตับ
ข้อมูลที่ใช้ประกอบการวินิจฉัย ได้แก่
1. ประวัติและการตรวจร่างกาย
1.1 อายุ, เพศ และภูมิลำเนา
=ผู้ป่วยอายุมากที่มีก้อนที่ตับ มีโอกาสเป็นมะเร็งสูงกว่าผู้ป่วยที่อายุน้อยกว่า.1
=เพศหญิง โดยเฉพาะอย่างยิ่งมีประวัติกินยาคุมกำเนิด ทำให้นึกถึงเนื้องอก hepatic adenoma.2
=ผู้ป่วยที่มีก้อนที่ตับและมีภูมิลำเนาอยู่ทางภาคตะวันออกเฉียงเหนือ ถ้ามีอาการตาเหลือง ตัวเหลืองร่วมด้วยอาจนึกถึงมะเร็งท่อน้ำดีในเนื้อตับ.
1.2 การติดเชื้อไวรัสตับอักเสบบี/ซี หรือภาวะตับแข็ง
=ผู้ป่วยที่มีประวัติการติดเชื้อไวรัสตับอักเสบบี/ซี และ/หรือมีภาวะตับแข็งตรวจพบว่ามีก้อนที่ตับให้สงสัยว่า ก้อนที่ตับเป็นมะเร็งตับชนิดปฐมภูมิแบบ hepatocellular carcinoma.2,3
1.3 ประวัติเป็นมะเร็งที่อื่นมาก่อน
=ผู้ป่วยที่มีประวัติเป็นมะเร็งที่อื่นมาก่อน และมีก้อนที่ตับให้สงสัยว่าก้อนที่ตับเป็นมะเร็งตับชนิดทุติยภูมิ (liver metastasis).2,3
1.4 อาการ (symptom)/อาการแสดง (sign)
=ในผู้ป่วยที่มีอาการของก้อนที่ตับ และการตรวจร่างกายพบว่า ตับโต มีโอกาสที่ก้อนที่ตับเป็นมะเร็งค่อนข้างสูง1
=ผู้ป่วยที่มีก้อนที่ตับ มีภาวะดีซ่าน คันตามตัว อุจจาระสีซีด ปัสสาวะสีเข้มอาจทำให้นึกถึงมะเร็งของท่อน้ำดีในเนื้อตับ. ผู้ป่วยที่มีไข้ ตับโต อาจมีฝีในตับ. การตรวจพบว่ามีภาวะตับแข็งอาจทำให้นึกถึงก้อนที่ตับว่าเป็น hepatocellular carcinoma. การตรวจพบต่อมน้ำเหลืองที่ supraclavicular ข้างซ้าย และ/หรือการตรวจทางทวารหนัก พบ rectal shelf ทำให้นึกถึงก้อนที่ตับว่าเป็น metastasis.
2. การตรวจทางห้องปฏิบัติการ
2.1 การตรวจหน้าที่การทำงานของตับ
Alkaline phosphatase จะสูงขึ้นในผู้ป่วยที่มีก้อนที่ตับเป็นมะเร็งมากกว่าผู้ป่วยที่มีก้อนที่ตับเป็นเนื้องอกไม่ร้ายแรง.1,3 นอกจากนี้การตรวจยังทำให้ทราบหน้าที่การทำงานของตับว่าดีมากน้อยเพียงพอหรือไม่.
2.2 Hepatitis B, C serology
2.3 Tumor marker
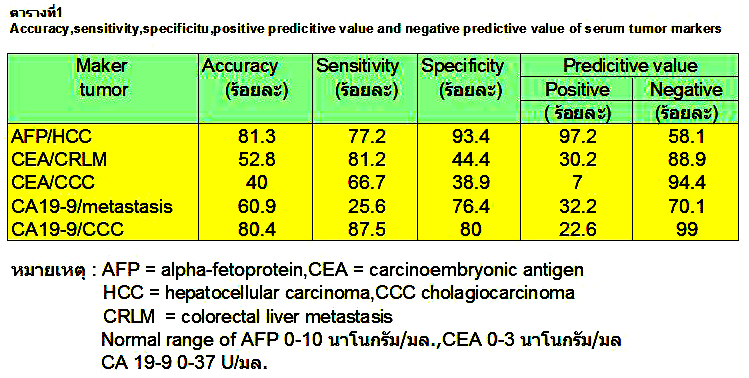
ร้อยละ 50-75 ผู้ป่วยที่มีก้อนที่ตับเป็นมะเร็งปฐมภูมิแบบ hepatocellular carcinoma จะมี serum alpha fetoprotein สูงกว่าปกติ.3,4 ผู้ป่วยที่มีก้อนที่ตับเป็นมะเร็งปฐมภูมิแบบ cholangio- carcinoma หรือมะเร็งทุติยภูมิจากมะเร็งลำไส้ใหญ่จะมี serum CEA และ/หรือ serum CA 19-9 สูงขึ้น1,3,4 ดังตารางที่ 14 แสดงความไวและความจำเพาะของ tumor marker ในการวินิจฉัยมะเร็งตับที่พบบ่อย.
3.การตรวจทางรังสีวิทยา
การตรวจพบก้อนที่ตับ นอกจากอาการทางคลินิกที่จะช่วยบ่งชี้แล้ว การตรวจทางรังสีวิทยาเป็นสิ่งจำเป็นอย่างยิ่งในการที่จะทำให้การวินิจฉัยมีประสิทธิภาพยิ่งขึ้น. ปัจจุบันวิวัฒนาการการพัฒนาทางด้านเทคโนโลยีได้ทำให้เครื่องมือที่ใช้ในการตรวจมีประสิทธิภาพสูงขึ้น. การตรวจทางรังสีวิทยาที่ใช้ใน การตรวจก้อนที่ตับมีอยู่หลายวิธี ได้แก่
1. Ultrasonography.
2. CT scan (spiral dynamic CT รวมถึง CT arterioportography).
3. MRI (dynamic MRI).
4. Liver scintigraphy.
5. Angiography.
Sensitivity, invasiveness (including radiation exposure), ต้นทุน และความแพร่หลายของการตรวจทางรังสีวิทยา สรุปได้ดังตารางที่ 2.5

3.1 Ultrasonography
อัลตราซาวนด์เป็นวิธีการสร้างภาพ non-invasive imaging ทำกันมากที่สุด. อัลตราซาวนด์สามารถแยกก้อนที่กลวงและตันออกจากกันได้ค่อนข้างดี.5 อย่างไรก็ดี sensitivity ของอัลตราซาวนด์ในการตรวจค้นพบ HCC ในผู้ป่วยโรคตับระยะสุดท้ายมีเพียงร้อยละ 50.6 นอกจากนี้ยังใช้อัลตราซาวนด์ในการเฝ้าติดตามการเปลี่ยนแปลงขนาดของก้อนในตับที่ไม่ใช่มะเร็ง เช่น hemangioma หรือ focal nodular hyperplasia.3
ข้อดีของอัลตราซาวนด์ คือ ราคาถูก, มีเครื่องมือใช้กันแพร่หลาย, ผู้ป่วยไม่ได้รับรังสี. ข้อจำกัดของอัลตราซาวนด์ คือ อาศัยความชำนาญของผู้ใช้, ความลำบากในการแปลผลภาพ, ผู้ป่วยอ้วนหรือมีแผลบริเวณช่องท้องด้านขวาบนทำให้การแปลผลและการตรวจเป็นไปด้วยความลำบากยากยิ่งขึ้น5
3.2 CT scan
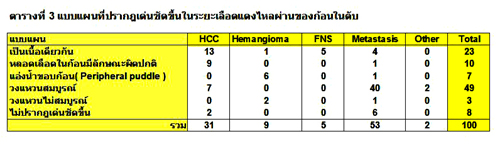
ปัจจุบันวิวัฒนาการทางด้านเทคโนโลยีดีขึ้นมาก ทำให้การตรวจด้วย CT scan ถูกพัฒนาขึ้นมาจนเป็น spiral CT scan ซึ่งสามารถตรวจช่องท้องด้านบนภายในเวลา 20-30 วินาที. นอกจากนี้ การทำ dynamic CT scan (arterial, portal, delayed enhancement phase) ช่วยบ่งบอกถึงธรรมชาติของก้อนในตับได้3,5-7 เช่น ก้อนที่แสดงได้ชัดเจนขึ้นในระยะการไหลของเลือดแดง (focal hypervascular lesion) ได้แก่ hepatocellular carcinoma, hepatic adenoma, focal nodular hyperplasia, hemangioma และ liver metastasis บางชนิด (ตารางที่ 3). เนื้องอกบางชนิดจะปรากฏเด่นชัดขึ้นใน delayed phase เช่น cholangiocarcinoma.
นอกจากนี้ยังมีการตรวจที่เรียกว่า CT arterial portography ซึ่งสามารถที่จะตรวจพบเนื้องอกที่มีขนาดเล็กกว่า 0.5 ซม.ได้. อย่างไรก็ดี การตรวจด้วยวิธีดังกล่าวนี้ใช้สำหรับการวางแผนการรักษาในการตัดเนื้องอกมากกว่าจะเป็นการคัดกรอง.5
3.3 MRI
MRI เหมาะที่จะใช้แยก cavernous hemangioma ออกจากเนื้องอกตับอื่นๆ ถึงร้อยละ 95 ของผู้ป่วย. นอกจากนี้ MRI ยังตรวจพบ metastatic islet cell, carcinoid, melanoma และเนื้องอก ไทรอยด์ได้ดีกว่า CT scan ที่สำคัญในกรณีที่ HCC พบร่วมกับภาวะตับแข็ง. ภาวะดังกล่าวนี้ MRI จะ ตรวจพบเนื้องอกได้ดีกว่า CT scan เพราะสามารถ แยก fatty infiltration และ regenerating nodule ได้ดีกว่า3
MRI ยังสามารถแยกถุงน้ำได้ รวมไปถึงบอกได้ว่าเลือดที่ออกเกิดขึ้นเฉียบพลัน, รองเฉียบพลัน หรือเรื้อรัง.5
3.4 Liver scintigraphy
Radionuclide scan จะตรวจค้นพบก้อนที่ตับได้ เมื่อเนื้องอกมีขนาดอย่างน้อย 2-2.5 ซม.3,5 เมื่อใช้ร่วมกับวิธีอื่นจะเหมาะกับการตรวจหาเนื้องอกที่เกี่ยวข้องกับหลอดเลือด เช่น hemangioma.
3.5 Angiography
เนื่องจากวิวัฒนาการในการตรวจด้วย CT scan และ MRI พัฒนาไปมาก ดังนั้นการตรวจด้วยวิธีนี้ทำกันลดน้อยลง และเสี่ยงต่อผู้ป่วยมากกว่าวิธีการตรวจอื่นๆ. อย่างไรก็ดี angiography ยังมีประโยชน์ โดยเฉพาะอย่างยิ่งในการเตรียมผู้ป่วยก่อนการทำผ่าตัด hepatic resection หรือใช้เป็นทางเลือกในการรักษา เช่น การทำ transarterial chemoembolization ใช้เป็นการตรวจในกรณีที่การตรวจวิธีอื่นๆ ไม่สามารถบอกได้ และก้อนที่ตับนั้นมีเลือดมาหล่อเลี้ยงมาก.3,5
4. การเจาะก้อนที่ตับตรวจ
การเจาะก้อนที่ตับเพื่อนำมาตรวจทางพยาธิวิทยานั้น สามารถบอกได้ว่าก้อนที่ตับนั้นเป็นอะไร. อย่างไรก็ดี วิธีการดังกล่าวค่อนข้าง invasive และมีภาวะแทรกซ้อนได้ เช่น อาการปวด อาการตกเลือดภายในช่องท้อง,10 ในรายที่เป็นมะเร็ง อาจมีการกระจายของเนื้องอกตามแนวของเข็มที่เจาะได้.10 ในผู้ป่วย hepatocellular carcinoma โอกาสเช่นนี้อาจสูงถึงร้อยละ 5.1.
นอกจากนี้ บางครั้งเซลล์ที่ได้ก็ไม่สามารถแยกโรคได้ โดยเฉพาะอย่างยิ่งการแยกโรค well differentiated hepatocellular carcinoma ออกจากเซลล์ตับที่ปกติ, focal nodular hyperplasia และ hepatic adenoma.2,10
Torzilli และคณะ12 ได้ทำการศึกษาถึงความแม่นยำในการตรวจก้อนที่ตับก่อนการผ่าตัด โดยอาศัยอาการทางคลินิก, tumor marker, การตรวจทางรังสีวิทยา (ultrasound, CT scan, MRI, angiography) โดยไม่มีการตรวจชิ้นเนื้อของก้อนที่ตับพบว่า มีความแม่นยำ, ความไว, ความจำเพาะในการตรวจก้อนที่ตับที่เป็น hepatocellular carcinoma (ร้อยละ 99.0, 100, 98.9)holangiocarcinoma (ร้อยละ 99.6, 100, 99.5), metastasis (ร้อยละ 99.1, 100, 98.8) และ benign liver tumor (ร้อยละ 98.7, 57.1, 100) ตามลำดับ.
ดังนั้นจะเห็นได้ว่า การเจาะก้อนที่ตับอาจจะมีความจำเป็นลดลง อย่างไรก็ดี ในผู้ป่วยที่มีก้อนที่ตับที่ยังไม่สามารถให้การวินิจฉัยได้และผู้ป่วยไม่แข็งแรงเพียงพอที่จะผ่าตัด การเจาะก้อนที่ตับอาจจะมีประโยชน์ในการวางแผนการรักษาต่อไป.2
5. การตรวจพิเศษทางห้องปฏิบัติการ
ในบางกรณี การตรวจทางห้องปฏิบัติการเป็นประโยชน์ เช่น การตรวจหา E.histolytica titer ในผู้ป่วยที่สงสัย amebic liver abscess, การตรวจ indirect hemagglutination test สำหรับ hydatid cyst.13
แนวทางในการวินิจฉัยและรักษาก้อนที่ตับ
แนวทางในการวินิจฉัยและรักษาก้อนที่ตับ แบ่งออกเป็น 4 ขั้นตอนดังนี้
ระยะที่ 1 การวินิจฉัยเบื้องต้น
ขั้นตอนนี้อาศัย อาการทางคลินิก, ผลเลือดจากการตรวจหน้าที่การทำงานของตับ, tumor marker, ไวรัสตับอักเสบบี, ซี รวมถึงการตรวจทางรังสีวิทยาขั้นต้น (อัลตราซาวนด์หรือ CT scan).
ระยะที่ 2 การตรวจทางรังสีพิเศษ
ขั้นตอนนี้มีวัตถุประสงค์เพื่อให้ได้การวินิจฉัยขั้นสุดท้าย รวมถึงการทราบระยะของโรคใน กรณีที่ก้อนที่ตับเป็นมะเร็ง. ขั้นตอนดังกล่าวนี้อาศัย การตรวจ CT scan, MRI, liver scintigraphy และการตรวจพิเศษต่างๆ เช่น การเจาะเลือดหาค่า E. histolytica titer เพื่อใช้ในการวินิจฉัย amebic liver abscess เป็นต้น.
ระยะที่ 3 การตรวจอย่าง invasive
หลังจากที่ผ่าน 2 ขั้นตอนจะสามารถวินิจฉัยก้อนที่ตับได้เป็นส่วนใหญ่ อย่างไรก็ดีมีก้อนที่ตับบางประเภทซึ่งยังไม่สามารถให้การวินิจฉัยได้ ในกรณีนี้อาจจะต้องได้รับการตรวจเพิ่มเติม เช่น การเจาะก้อนที่ตับเพื่อนำชิ้นเนื้อไปตรวจ, การทำ angiography หรือแม้แต่การผ่าตัดเนื้องอกในผู้ป่วยบางรายซึ่งจะ กล่าวต่อไปในภายหลัง.
ระยะที่ 4 การวางแผนรักษา
หลังจากวินิจฉัยโรคได้ ทำการวางแผนการรักษาต่อไป.
ระยะที่ 1 การวินิจฉัยเบื้องต้น
เมื่อผู้ป่วยผ่านขั้นตอนนี้ จะแบ่งก้อนที่ตับออกได้เป็น 3 กลุ่มใหญ่ๆ ดังนี้
กลุ่มที่ 1 ก้อนที่สงสัยเป็นเนื้องอกไม่ร้ายแรง เช่น liver cyst หรือ cavernous hemangioma.
กลุ่มที่ 2 ก้อนที่สงสัยเป็นมะเร็ง เช่น hepatocellular carcinoma ในผู้ป่วยที่มีภาวะตับแข็งหรือติดเชื้อไวรัสตับอักเสบบี/ซี และมีค่า alphafetoprotein (AFP) ขึ้นสูง โดยเฉพาะอย่างยิ่งค่าที่มากกว่า 400 นาโนกรัม/มล.,14 liver metastasis ในผู้ป่วยที่มีประวัติ primary cancer ที่อื่น เช่น มะเร็งลำไส้ใหญ่และมีค่า CEA ขึ้นสูงกว่าค่าปกติ, cholangiocar cinoma (intrahepatic type) ในผู้ป่วยที่มีภูมิลำเนามาจากทางภาคตะวันออกเฉียงเหนือและมีอาการดีซ่านอุดกั้น.
กลุ่มที่ 3 ไม่สามารถระบุได้ว่าก้อนที่ตับ เป็นเนื้องอกชนิดใด เช่น ก้อนที่ตับเป็นก้อนตัน หรือ กลุ่มที่ไม่ใช่ถุงน้ำทั่วไป เช่น ถุงน้ำจากพยาธิ หรือจากมะเร็ง.
ระยะที่ 2 การตรวจทางรังสีพิเศษ
หลังจากผู้ป่วยได้รับการตรวจเพิ่มในขั้นตอนนี้ เช่น การทำ CT scan หรือ MRI ก้อนที่ตับส่วนใหญ่ จะสามารถวินิจฉัยได้ว่าเป็นเนื้องอกชนิดไม่ร้ายแรง เช่น ฝีที่ตับ, hemangioma, parasitic cyst, focal fatty infiltration/sparing. ก้อนที่ตับเป็นมะเร็ง เช่น hepatocellular carcinoma, liver metastasis, cholangiocarcinoma ซึ่งนอกจากจะได้การวินิจฉัยขั้นสุดท้ายยังสามารถทราบระยะของโรค (staging) และช่วยวางแผนในการผ่าตัดด้วย (mapping). อย่างไรก็ดี ก้อนที่ตับบางชนิดที่ยังไม่สามารถบอกชนิดของก้อนได้ต้องผ่านขั้นตอนที่ 3.
ระยะที่ 3 การตรวจอย่าง invasive
ก้อนที่ตับกลุ่มนี้ โดยเฉพาะอย่างยิ่งกลุ่มที่เป็นเนื้องอกไม่ร้ายแรง เช่น focal nodular hyperplasia, adenoma, hemangioma หรือถุงน้ำ ในผู้ป่วยกลุ่มนี้ การเจาะก้อนที่ตับนอกจากจะไม่ได้ประโยชน์ในการวินิจฉัยแล้ว ยังอาจเพิ่มความเสี่ยงได้. ผู้ป่วยกลุ่มนี้การผ่าตัดตัดเนื้องอกออก นอกจากจะทำให้ได้ การวินิจฉัยแล้ว ยังเป็นการรักษาไปพร้อมๆ กันด้วย.
ในผู้ป่วยที่สงสัยเป็น cholangiocarcinoma และมีอาการของดีซ่านอุดกั้นการทำ percutaneous transhepatic biliary drainage (PTBD) นอกจากจะทราบถึงกายวิภาคของทางเดินน้ำดีแล้ว ยังช่วยบรรเทาอาการดีซ่าน.
การเจาะก้อนที่ตับอาจจะทำในขั้นตอนนี้ โดยเฉพาะอย่างยิ่งในผู้ป่วยที่จะวางแผนการรักษาโดยวิธีการไม่ผ่าตัด หรือก้อนที่ตับที่ยังไม่สามารถวินิจฉัย โรคได้.
ระยะที่ 4 การวางแผนรักษา
ในกรณีเนื้องอกไม่ร้ายแรง และไม่มีอาการใช้การเฝ้าติดตาม. อย่างไรก็ดีในกรณีที่มีอาการ เช่น อาการปวด หรือมีภาวะแทรกซ้อน เช่น การติดเชื้อ, แตก, เลือดออกภายในก้อนหรือมีโอกาสเป็นมะเร็ง (ในกรณีของ hepatic adenoma) หรือก้อนที่ตับที่ไม่สามารถแยกโรคได้ (โดยเฉพาะอย่างยิ่งกลุ่ม benign liver tumor) การรักษาคือ การผ่าตัด. สำหรับกรณีของก้อนที่ตับเป็นมะเร็ง การรักษาที่ดีที่สุดคือ การผ่าตัด โดยเกณฑ์ที่ใช้ในการผ่าตัด คือ ผู้ป่วยแข็งแรงเพียงพอที่จะผ่าตัด ตับเหลือเพียงพอที่จะทำงานเป็นปกติภายหลังการผ่าตัด ก้อนที่ตับสามารถผ่าตัดเอา ออกได้หมด (ยกเว้นเนื้องอกบางชนิดถึงแม้จะเอาออกไม่หมดแต่คุณภาพชีวิตภายหลังการผ่าตัดดีขึ้น เช่น เนื้องอกกลุ่มneuroendocrine tumor, carcinoid syndrome) และไม่มีการแพร่กระจายของเนื้องอกออกนอกตับ (ยกเว้นในบางกรณี ถึงแม้จะมีการกระจายของมะเร็งนอกตับ เช่น มะเร็งของลำไส้ใหญ่กระจายมาที่ปอด แต่ถ้าสามารถผ่าตัดเอาเนื้องอกที่ปอดออกได้ก็อาจพิจารณาผ่าตัดก้อนที่ตับได้). กรณีถ้าก้อนที่ตับเป็นมะเร็ง แต่ไม่สามารถผ่าตัดได้ การรักษาขึ้นอยู่กับลักษณะของเนื้องอกชนิดนั้นๆ เช่น การให้เคมีบำบัด, การฉายแสง, การทำ transarterial chemoembolization (TACE), การใช้ radiofrequency ablation หรือการรักษาอาการดีซ่าน เป็นต้น.
สรุปแนวทางในการวินิจฉัยและรักษาก้อนที่ตับนั้น ได้เป็นแผนภูมิที่ 1 และ 2.
เอกสารอ้างอิง
1. Little JM, Kenny J, Hollands MJ. Hepatic incidentalo-ma : a modern Problem. World J Surg 1990;14:448-51.
2. Lise M, Pian PP, Nitti D, Miotto D, Balduino M, Bacchetti S. Benign liver tumors in adults : diagnosis and management. J Hep Bil Pancr Surg 1996;3:89-97.
3. Quinlan RM. Tumors of the liver. In : Zuidema GD, ed. Shackelfords surgery of the alimentary tract. 4th ed. London, Philadelphia, Sleisenger-Fordtran : WB Saunders Company Ltd, 1996:512-25.
4. Torzilli G, Makuuchi M, Ferrero A, et al. Accuracy of the preoperative determination of tumor markers in the differentiation of liver mass lesions in surgical patients. Hepatogastroenterlogy 2002;49:740-45.
5. Bennett WF, Bova JG. Review of hepatic imaging and a problem-oriented approach to liver mass. Hepatology 1990;12:761-75.
6. Foster JH. Benign liver tumors. World J Surg 1982;6:25-31.
7. Horton KM, Bluemke DA, Hruban RH, Soyer P, Fishman EK. CT and MR Imaging of benign hepatic and biliary tumors. Radiographics 1999;19:431-51.
8. Reddy KR, Schiff ER. Approach to a liver mass. Sem Liv Dis 1993;13:423-35.
9. Rubin RA, Mitchell DG. Evaluation of the solid hepatic mass. Med Clin NA 1996;80:907-28.
10. Souto E, Gores GJ. When should a liver mass suspected of being a hepatocellular carcinoma be biopsied? Liver Transpl 2000;6:73-5.
11. Takamori R, Wong LL, Dang C, Wong L. Needle tract implantation from hepatocellular cancer : Is needle biopsy of the liver always necessary? Liver Transpl 2000;6:67-72.
12. Torzilli G, Minagawa M, Takayama T, et al. Accurate preoperative evaluation of liver mass lesions without fine needle biopsy. Hepatology 1992;30:889-93.
13. Taylor BR, Langer B. Current surgical management of hepatic cyst disease. Adv Surg 1998;31:127-48.
14. Bruix J, Sherman M, Llovet JM, et al. Clinical management of hepatocellular carcinoma. Conclusions of the Barcelona-2000 EASL conference. J Hepatol 2000;35:421-30.
บุญชู ศิริจินดากุล พ.บ., ภาควิชาศัลยศาสตร์, คณะแพทยศาสตร์, จุฬาลงกรณ์มหาวิทยาลัย
- อ่าน 40,125 ครั้ง
 พิมพ์หน้านี้
พิมพ์หน้านี้




