แนวทางการดูแลรักษาผู้ป่วยนอก โรคธัยรอยด์ผิดปกติ : Hyperthyroidism และ Hypothyroidism
การทำงานผิดปกติของต่อมธัยรอยด์ พบได้บ่อยในเวชปฏิบัติ อัตราส่วนผู้ป่วยหญิง ต่อชาย ประมาณ 4 : 1 อุบัติการณ์ของภาวะ hypothyroidism และ thyrotoxicosis เท่ากับ 3.5/1000 และ 0.8/1000 ตามลำดับ แม้ไม่มีข้อมูลชัดเจนว่าผู้ป่วยกลุ่มโรคดังกล่าวมีอายุขัยเฉลี่ยสั้นลง แต่ด้วยเป็นปัญหาที่สำคัญในเวชปฏิบัติ และเป็นกลุ่มโรคที่ต้องดูแลต่อเนื่องระยะยาว จึงจะได้นำเสนอแนวทางเวชปฏิบัติสำหรับกลุ่มโรคธัยรอยด์โดยสรุป ดังต่อไปนี้
บทบาทการตรวจคัดกรองกลุ่มโรคธัยรอยด์
► การตรวจระดับฮอร์โมนธัยรอยด์เป็นวิธีการที่ไม่แนะนำในประชากรทั่วไป ไม่แนะนำในผู้ป่วยที่ถูกรับไว้ในโรงพยาบาลด้วยโรคอื่น ยกเว้นแต่สงสัยภาวะธัยรอยด์ผิดปกติ แต่อาจมีประโยชน์ในกลุ่มเด็กแรกเกิด (อุบัติการณ์ 1:2700) หญิงตั้งครรภ์ (2/1000) หญิงระยะหลังคลอด ผู้ป่วยที่ได้รับยา lithium หรือยา amiodarone ผู้ป่วยที่เคยได้รับการผ่าตัด ต่อมธัยรอยด์หรือเคยกลืน แร่เพื่อรักษาภาวะธัยรอยด์เป็นพิษและในกลุ่มผู้สูงอายุ.
► การตรวจอัลตราซาวนด์ต่อมธัยรอยด์เป็นวิธีการที่ไม่แนะนำในประชากรทั่วไป.
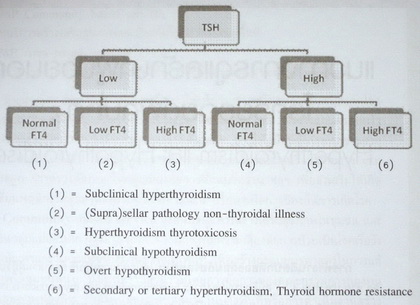
การวินิจฉัยการแปลผลเลือด และการตรวจเพิ่มเติมที่จำเป็น
การแปลผลเลือด
โดยทั่วไป อาจใช่ความสัมพันธ์ระหว่างค่า TSH และ FT4 ในการแปรผลเลือดดังแผนภาพ
อย่างไรก็ดี มีข้อพิจารณาการเลือกตรวจ การทำงานของต่อมธัยรอยด์เบื้องต้น โดยอาจเลือกใช้ T3 แทน FT4 เพราะอุบัติการณ์ภาวะ T3 toxicosis (16.02 %) มากกว่า T4 toxicosis (2.91 %) ทั้งนี้ประสิทธิภาพการวัดระดับ T3 มีค่าความไวร้อยละ 97.57 และค่าความจำเพาะร้อยละ 100 เทียบกับการวัดระดับ T4 และการวัด TSH ซึ่งมีความไวร้อยละ 83.98 และความจำเพาะร้อยละ 100.
สำหรับการตรวจ Thyroid autoantibodies (TSH receptor antibodies/Thyroid stimulating immunoglobulin) หรือ Thyroid Scintigraphy (123I หรือ 99m Tc) เพื่อวินิจฉัยสาเหตุภาวะธัยรอยด์เป็นพิษนั้น ก่อนเริ่มรักษา ควรพิจารณาทำอย่างยิ่งสำหรับผู้ป่วยต่อไปนี้ (1) ผู้ที่มีภูมิลำเนาจากพื้นที่ที่ มีปัญหาเรื่องภาวะขาดธาตุไอโอดีน (2) ผู้สูงอายุที่มีประวัติคอโตมานาน หรือ (3) กลุ่มที่มีลักษณะของ Graves' disease ไม่ชัดเจน. เนื่องจากแต่ละกลุ่มโรคมีวิธีการรักษาที่แตกต่างกัน ดังจะได้กล่าวต่อไป

ทางเลือกการรักษา
1. ภาวะธัยรอยด์เป็นพิษ
ประเทศสหรัฐอเมริกา Graves' disease และ toxic nodular goiter พบได้ร้อยละ 60 และร้อยละ 15-20 ตามลำดับ. สำหรับประเทศไทย ตัวเลขอุบัติการณ์ของทั้งสองโรคน่าจะต่างไป เนื่องจากยังมีบางพื้นที่ที่ประสบปัญหาขาดธาตุไอโอดีนซึ่งเป็นความเสี่ยงเกิดภาวะ toxic nodular goiter.
แนวทางการรักษาภาวะธัยรอยด์เป็นพิษ แต่ละชนิดเป็นดังนี้
► Graves' disease : สามารถเลือกใช้ ทั้งการรักษาด้วยยา, radioactive iodine หรือการผ่าตัดในประเทศสหรัฐอเมริกาเลือกใช้ Radioactive iodine (กลืนแร่) เป็นหลัก เนื่องจากตามธรรมชาติของโรคจะกลับเป็นซ้ำได้ค่อนข้างมาก ถึงร้อยละ 50-60 (คิด cumulative) หากใช้การรักษาด้วยยาเป็น ทางเลือกแรก. สำหรับในประเทศไทยและบางประเทศ ในยุโรปยังคงใช้การรักษาด้วยยาเป็นทางเลือกแรกยกเว้นในกรณีที่ก้อนโตมากอาจพิจารณาใช้การผ่าตัดรักษา. ผู้ป่วยที่มีปัญหา Graves orbitopathy ร่วมด้วย ควรพิจารณาให้การรักษาด้วยยา เพราะการกลืนแร่ อาจทำให้อาการดังกล่าวเลวลงได้ (ร้อยละ 15). ข้อเตือนใจสำคัญประการหนึ่งคือ การกลืนแร่ไม่ปลอดภัยสำหรับหญิงตั้งครรภ์และหญิงให้นมบุตร.
หมายเหตุ : ค่าบริการรังสีรักษา (กลืนแร่) ตามอัตราโรงพยาบาลศิริราชราคา 3,000 บาท
► Toxic nodular : ควรเลือกใช้การกลืนแร่ หรือการผ่าตัดเป็นหลักเนื่องจากไม่สามารถหวังผลหายขาดได้จากการรักษาด้วยยา.
► Subacute thyroiditis ควรได้รับการ รักษาตามอาการด้วย aspirin และ beta blockers.
► สำหรับสาเหตุที่พบไม่บ่อยอื่นๆ ของ ภาวะธัยรอยด์เป็นพิษ เช่น iodine excess, pituitary tumor, molar pregnancy, metastatic thyroid carcinoma, struma ovarii, amiodarone induced thyrotoxicosis จะขอละไว้ไม่กล่าวในที่นี้.
2. ภาวะ subclinical hyperthyroidism
เป็นภาวะที่มีส่วนเพิ่มอัตราการเกิด atrial fibrillation อย่างมีนัยสำคัญทางสถิติ. อย่างไรก็ดี มีข้อมูล ไม่เพียงพอว่าภาวะดังกล่าวมีผลทำให้อัตราตายเพิ่มขึ้น ดังนั้นควรพิจารณารักษาก็ต่อเมื่อ ผู้ป่วยอายุมากกว่า 60 ปี, หญิงหมดประจำเดือน ที่ระดับ TSH < 0.1 mU/l, ผู้ป่วยอื่นๆ ที่มีอาการพิษธัยรอยด์, atrial fibrillation หรือ osteopenia.
3. Primary hypothyroidism
สาเหตุส่วนใหญ่ของภาวะนี้คือ Hashimoto thyroidits (ข้อมูลสหรัฐอเมริกา). การให้ฮอร์โมนทดแทน (levothyroxine) เป็นวิธีการรักษาหลัก ทั้งนี้ สามารถเริ่มให้การรักษาด้วยยาเต็มขนาด คือ 1.6-2 ไมโครกรัมต่อน้ำหนักตัว 1 กิโลกรัมได้เลยในหญิง ตั้งครรภ์ ผู้ป่วยอายุน้อยและไม่มีโรคประจำตัวอื่น แต่ในผู้ป่วยสูงอายุหรือมีปัญหาโรคหัวใจและหลอดเลือดควรค่อยๆ ปรับขนาดยาขึ้นโดยเริ่มที่ 12.5 ไมโครกรัม. สำหรับผู้ป่วยที่มีภาวะธัยรอยด์ต่ำตั้งแต่ก่อนตั้งครรภ์ ควรพิจารณาปรับขนาดยาเพิ่มขึ้นร้อยละ 30 เมื่อเริ่มตั้งครรภ์.
4. ภาวะ subclinical hypothyroidism
มีอุบัติการณ์ประมาณร้อยละ 1-10 ในกลุ่มประชากรวัยผู้ใหญ่ แต่มีข้อมูลไม่แน่ชัดในการพิจารณาเริ่มการรักษา ยกเว้นในหญิงตั้งครรภ์ซึ่งควรรักษาทันทีในรายที่มี TSH >4.0 mU/l โดยอาจใช้ระดับ TSH คาดคะเนได้ว่าผู้ป่วยมีแนวโน้มเกิดภาวะธัยรอยด์ต่ำ (overt hypothyroidism) มากน้อยเพียงไร ดังนี้
1) TSH< 6.0 mU/l โอกาสเกิดภาวะธัยรอยด์ต่ำน้อยมาก.
2) TSH 6-12 mU/l มีโอกาสเกิดภาวะธัยรอยด์ต่ำร้อยละ 42.8.
3) TSH >12 mU/l มีโอกาสเกิดภาวะธัยรอยด์ต่ำร้อยละ 76.9.
การเลือกใช้ยาและข้อควรระวัง
ยาต้านธัยรอยด์ที่ใช้แพร่หลายในปัจจุบันมี 2 ชนิด คุณสมบัติโดยเปรียบเทียบดังตารางที่ 1.
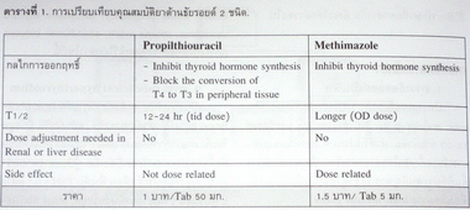
ผลข้างเคียงที่อันตรายและพึงระวังของยากลุ่มนี้ ได้แก่
1. Agranulocytosis ส่วนใหญ่มักเกิดในช่วง 90 วันแรกหลังเริ่มรักษาและควรระวังมากขึ้นในผู้ป่วยสูงอายุ. ผู้ป่วยมักมาด้วยอาการไข้ เจ็บคอ การเพาะเชื้อในเลือดพบ P. aeruginosa บ่อยที่สุด อัตราการเกิดใกล้เคียงกันในผู้ป่วยที่ได้รับ PTU และ methimazole (0.35 และ 0.37 ตามลำดับ).
แม้ภาวะดังกล่าวมีอันตรายถึงชีวิต แต่ไม่มีการศึกษายืนยันประโยชน์คุ้มค่าในการตรวจ CBC เพื่อเฝ้าระวังภาวะนี้.
2. Hepatotoxicity บ่งชี้โดยค่า aminotransferase เพิ่มขึ้นได้ประมาณ 1.1-6 เท่าของค่าปกติ อุบัติการณ์ของภาวะนี้ประมาณร้อยละ 0.1-0.2 ใน ผู้ป่วยที่ได้รับ PTU ส่วนมากพบหลังเริ่มการรักษาประมาณ 3 เดือน. สำหรับผู้ป่วยที่ได้รับ methimazole ปัญหาจะปรากฏในรูปของ cholestasis และ periportal imflammation. อย่างไรก็ตาม ยังไม่มีการศึกษายืนยันประโยชน์คุ้มค่าในการตรวจ Liver function test เพื่อเฝ้าระวังภาวะนี้.
3. Vasculitis พบได้บ่อยกว่าในผู้ป่วยที่ได้รับ PTU.
4. Congentital anomalies ได้แก่ ภาวะ aplasia cutis, choanal/esophageal atresia ในหญิงตั้งครรภ์ที่ได้รับ methimazole ดังนั้น จำเป็นอย่างยิ่งที่จะต้องแนะนำผู้ป่วยหญิงที่ได้รับ methimazole ในเรื่องการคุมกำเนิด และเมื่อผู้ป่วยต้องการตั้งครรภ์ควรเปลี่ยนไปใช้ PTU แทนทั้งนี้อาจใช้ dose potency ratio = 10 : 1 (methimazole 30 มก. : PTU 300 มก.) อ้างอิงในการ switch ยา.
แนวทางการดูแลรักษาต่อเนื่อง
► ผู้ป่วยที่ได้รับการรักษาภาวะธัยรอยด์เป็นพิษโดยการใช้ยาต้านธัยรอยด์ควรได้รับยาต่อเนื่องอย่างน้อย 12-18 เดือนจึงพิจารณาหยุดยา นอกจากนี้ควรตรวจการทำงานของต่อมธัยรอยด์ เพื่อพิจารณาปรับยาทุก 4-6 สัปดาห์ เมื่อได้ค่าตามเป้าหมายสามารถขยายระยะเวลาตรวจเลือดเป็น ทุก 3 เดือนได้.
► ควรพิจารณาให้ calcium และ bisphosphonate เสริมในผู้ป่วยธัยรอยด์เป็นพิษซึ่งเป็นหญิงสูงอายุ และมีภาวะกระดูกพรุน.
► สำหรับภาวะธัยรอยด์ต่ำ หลังเริ่มให้ฮอร์โมนทดแทนควรตรวจเลือดทุก 4-6 สัปดาห์เช่นเดียวกัน เมื่อได้ระดับแล้วสามารถขยายเวลาได้เป็นทุก 1 ปีในกรณีที่ TSH ปกติแต่ยังมีอาการแสดงของภาวะธัยรอยด์ต่ำ ให้ปรับยาขึ้นได้อีกโดยมุ่งให้ TSH อยู่ในระดับปกติค่อนไปทางต่ำ สำหรับในหญิงตั้งครรภ์ควรพิจารณาปรับยาให้ TSH อยู่ในระดับปกติค่อนไปทางสูง.
► สำหรับผู้ป่วยที่เลือกวิธีรังสีรักษาแต่ได้รับยาต้านธัยรอยด์อยู่ในช่วงแรก ควรหยุด methimazole อย่างน้อย 3-5 วัน หรือ PTU อย่างน้อย 15 วัน ก่อนกลืนแร่.
► หลังการกลืนแร่รักษาภาวะธัยรอยด์เป็นพิษ ห้ามผู้ป่วยตั้งครรภ์เป็นเวลาอย่างน้อย 6 เดือน.
► ผู้ป่วยโรคธัยรอยด์เป็นพิษซึ่งต่อมาตั้งครรภ์ แม้ว่าจะควบคุมเป็น euthyroid แล้ว ควรพิจารณาส่งตรวจ TSH receptor antibodies เพื่อประเมินความเสี่ยงของทารกในครรภ์ด้วย.
► ในหญิงตั้งครรภ์ ภาวะ gestational transient hyperthyroidism มักหายไปได้เองหลังสัปดาห์ที่ 18 สำหรับภาวะธัยรอยด์เป็นพิษส่วนใหญ่สามารถหยุดยาได้ในช่วงไตรมาสที่สาม.
► ในหญิงให้นมบุตรสามารถเลือกใช้ได้ทั้ง methimazole (< 20 มก./วัน) และ PTU < 300 มก./วัน).
เด่นหล้า ปาลเดชพงศ์ พ.บ.
สาขาวิชาการบริบาลผู้ป่วยนอก
ภาควิชาอายุรศาสตร์ คณะแพทยศาสตร์ศิริราชพยาบาล
มหาวิทยาลัยมหิดล
- อ่าน 76,418 ครั้ง
 พิมพ์หน้านี้
พิมพ์หน้านี้




