ภาพที่ 1. พาร์กินโซนิซึมมีได้หลายสาเหตุ โดยที่โรคพาร์กินสัน เป็นสาเหตุที่พบบ่อยที่สุด มากถึงร้อยละ 70.
พาร์กินโซนิซึม (parkinsonism) เป็นกลุ่มอาการ (syndromes) ไม่ใช่โรค (ต่างจากโรคพาร์กินสันที่จะกล่าวโดยละเอียดในภายหลัง) ที่รวมถึงลักษณะอาการสั่นที่มือหรือขาขณะอยู่เฉย (rest tremor) อาการเคลื่อนไหวช้า (bradykinesia) อาการแข็งเกร็ง (rigidity) และปัญหาในเรื่องของการทรงตัว (postural instability) (ตารางที่ 1). ผู้ป่วยพาร์กินโซนิซึมโดยส่วนใหญ่อาจมีอาการไม่ครบทั้ง 4 อาการตามที่กล่าวไว้ข้างต้น แต่อย่างน้อยควรจะมีอย่างน้อย 2 อาการก่อนที่จะเรียกว่า ผู้ป่วยท่านนั้นมีอาการของพาร์กินโซนิซึม (probable parkinsonism).
ภาพที่ 2. Basal ganglia circuitry ประกอบด้วย 2 pathways หลัก เรียกว่า direct และ indirect pathways ใน direct pathway สัญญาณที่ส่งออกจาก striatum จะยับยั้ง GPi และ SNr ใน indirect pathway จะมีสัญญาณยับยั้ง ระหว่าง striatum และ GPe ต่อด้วย GPe และ STN ผลลัพธ์สุดท้าย คือการเพิ่มสัญญาณการยับยั้งจาก GPi/SNr ไปยัง ventral lateral nucleus ของ thalamus ส่งผลให้สัญญาณกระตุ้นจาก ventral lateral nucleus ของ thalamus ไปยัง cortex น้อยลง ทำให้ผู้ป่วยพาร์กินสันมีอาการเคลื่อนไหวช้าและแข็ง.
ภาพที่ 3. ภาพของ Lewy body.
ภาพที่ 4. Pathway ของ dopamine biosynthesis.
ภาพที่ 5. ลักษณะการเขียนตัวหนังสือที่เล็ก และชิดติดกัน เรียกว่า micrographia.
ภาพที่ 6. ภาพ MRI ของผู้ป่วย vascular parkinsonism แสดงถึงรอยโรครอบโพรงสมอง.
อาการพาร์กินโซนิซึมพบบ่อยหรือไม่ สถิติที่ได้ศึกษาไว้และน่าเชื่อถือจะเป็นที่ Omstead County ศึกษาโดย Mayo Clinic ที่มลรัฐ Rochester ประเทศสหรัฐอเมริกา โดยพบว่าอัตราของพาร์กินโซนิซึมเพิ่มตามอายุ โดยจะพบเพียง 0.8/105 ในประชากรอายุระหว่าง 0-29 ปี แต่จะเพิ่มขึ้นเรื่อยๆ เป็น 25.6/105 ในประชากรอายุระหว่าง 50-59 ปี และมากเพิ่มขึ้น 11 เท่า (304.8/105) ในประชากรที่อายุระหว่าง 80-99 ปี.1 อัตราเสี่ยงของการเกิดพาร์กินโซนิซึม (lifetime risk) จะอยู่ประมาณร้อยละ 3.7-4.4 โดยจะสูงในผู้ชายมากกว่าผู้หญิงเล็กน้อย.2
สาเหตุของพาร์กินโซนิซึม
ดังที่ได้กล่าวไว้ข้างต้น พาร์กินโซนิซึมเป็นกลุ่มอาการ เพราะฉะนั้นจึงมีได้หลายสาเหตุ (ตารางที่ 2) ซึ่งโรคพาร์กินสันเป็นสาเหตุที่พบบ่อยที่สุดของอาการพาร์กินโซนิซึม ประมาณร้อยละ 77 (ภาพที่ 1). สาเหตุที่พบบ่อยเป็นอันดับ 2 รองมาจากโรคพาร์กินสัน คือ อาการพาร์กินโซนิซึมที่เกิดจากยาบางชนิด (drug-induced parkinsonism) สาเหตุอื่นๆ นอกจากนี้จะพบน้อยซึ่งได้แก่กลุ่มโรค ความเสื่อมทางระบบประสาทต่างๆ ที่มีอาการพาร์กินโซนิซึมเป็นส่วนประกอบ ดังเช่น Parkinsonism plus syndromes หรือกลุ่มโรคทางพันธุกรรมบางโรค ที่จะกล่าวโดยละเอียดต่อไป. เนื่องจากโรคพาร์กินสันเป็นสาเหตุของพาร์กินโซนิซึมที่พบบ่อยที่สุด และมีการรักษาในปัจจุบันที่ได้ผลดี จึงจะขอกล่าวถึงก่อน. การวินิจฉัยโรคพาร์กินสันได้ถูกต้อง โดยเฉพาะการเริ่มรักษาตั้งแต่ในระยะเริ่มแรกอย่างเหมาะสม จะส่งผลให้ผู้ป่วยมีคุณภาพชีวิตที่ดีขึ้น ซึ่งยังส่งผลไปถึงครอบครัวผู้ป่วยเองและผู้ที่อยู่รอบข้าง.


โรคพาร์กินสัน (Parkinson's disease)
โรคพาร์กินสัน (Parkinson's disease) เป็นโรคความเสื่อมของระบบประสาท (neurodegenerative disorders) ที่พบได้บ่อยรองลงมาจากโรคหลงลืม หรือโรคอัลไซเมอร์. ชื่อโรคพาร์กินสันได้มาจากชื่อของนายแพทย์เจมส์ พาร์กินสัน แพทย์ ชาวอังกฤษ ซึ่งเป็นแพทย์คนแรกที่ได้พูดถึงอาการของโรคนี้ในปี พ.ศ. 2360 ในบทความที่ชื่อว่า Shaking Palsy. โรคพาร์กินสันเกิดขึ้นในทั้งผู้ชายและ ผู้หญิงในอัตราส่วนที่ใกล้เคียงกัน หรือมากกว่าใน ผู้ป่วยชายเพียงเล็กน้อย อายุเฉลี่ยของผู้ป่วยโรค พาร์กินสันจะอยู่ประมาณ 55-60 ปี และผู้ป่วยโดยส่วนมากจะมีอายุมากกว่า 50 ปี. ผู้ป่วยพาร์กินสันที่อายุน้อยหรือ Young-onset Parkinson's disease (YOPD) หมายถึง ผู้ป่วยที่มีอาการของโรคพาร์ กินสันก่อนอายุ 40 ปี ซึ่งผู้ป่วยในกลุ่มนี้จะมีพยาธิสภาพเช่นเดียวกับผู้ป่วยพาร์กินสันอายุมากแต่จะ มีการดำเนินโรคที่แตกต่างไป. ส่วน Juvenile parkinsonism (JP) หมายถึง กลุ่มผู้ป่วยที่มีอาการ พาร์กินโซนิซึม (parkinsonism) ซึ่งรวมถึงการเคลื่อนไหวช้า สั่น เกร็ง ในอายุที่น้อยกว่า 20 ปี. JP เป็นกลุ่มอาการที่ยังรวมไปถึงโรคอื่นๆ ที่นอกเหนือไปจาก autosomal recessive Parkinson's disease ดังเช่น Dopa responsive dystonia (DRD), Wilson's disease, หรือ Juvenile Huntington's disease เป็นต้น.
สถิติอัตราการเกิดของโรคพาร์กินสันที่มีรายงานในปัจจุบันส่วนใหญ่เป็นการศึกษาในผู้ป่วย Caucasian และข้อมูลในผู้ป่วยเอเชีย รวมถึงผู้ป่วยไทยยังมีไม่มาก ซึ่งรายงานส่วนใหญ่จะอยู่ประมาณ 4.5-19 ต่อประชากร 100,000 คน ถ้าดูเฉพาะความชุกของโรคพาร์กินสันในประชากรที่อายุมากกว่า 65 ปีขึ้นไป ก็จะได้ตัวเลขจำง่ายๆ ก็คือ ในประชากรที่อายุมากกว่า 65 ปี 100 คน จะพบผู้ป่วยโรคพาร์กินสัน 1 คน. ปัจจัยหลายอย่างอาจส่งผลทำให้เกิดโรคพาร์กินสัน ได้ง่ายขึ้น เนื่องจากโรคพาร์กินสันส่วนมากเกิดในผู้สูงอายุ อายุที่มากขึ้นจึงจัดว่าเป็นปัจจัยเสี่ยงที่ชัดเจนอย่างหนึ่งในโรคพาร์กินสัน. ประวัติครอบครัวของโรคพาร์กินสันมีส่วนเพิ่มความเสี่ยงต่อโรคในทางสถิติ ในขณะที่อัตราความเสี่ยงของโรคพาร์กินสันจะเพิ่มเพียงเล็กน้อย ในผู้ป่วยที่อายุมากกว่า 50 ปี อัตราความเสี่ยงจะเห็นได้ชัดเจนมากขึ้น ถ้าเป็นผู้ป่วยในกลุ่ม YOPD หรือ JP ซึ่งความเสี่ยงของโรคจะเพิ่มอย่างชัดเจน ถ้าญาติใกล้ชิด โดยเฉพาะพี่น้องเป็นโรคพาร์กินสัน (first-degree relative). การศึกษาทางพันธุกรรมในปัจจุบันได้ค้นพบถึง ความผิดปกติทางพันธุกรรมที่ส่งผลให้เกิดโรคพาร์กินสันในอายุน้อย ในบางครอบครัว ดังเช่น Parkin mutations, UCLH1 หรือ PINK1 mutations เป็นต้น. การค้นพบ Parkin mutation ช่วยอธิบายถึงสาเหตุการเกิดโรคพาร์กินสัน ในผู้ป่วยที่อายุน้อย โดยเฉพาะ Parkin mutation เป็นสาเหตุในร้อยละ 75 ของผู้ป่วยที่มี early-onset parkinsonism ก่อนอายุ 20 ปี.
พยาธิสภาพและสาเหตุของโรคพาร์กินสัน
โรคพาร์กินสันเกิดจากการเสื่อมตายของเซลล์ในส่วนที่เรียกว่า substantia nigra โดยเฉพาะในส่วนของ substantia nigra pars compacta (SNc). สาเหตุที่เป็นต้นเหตุให้เกิดการเสื่อมของส่วน SNc ยังไม่เป็นที่ทราบแน่นอน การเสื่อมของสมองในส่วนนี้ส่งผลต่อการทำงานที่ต่อเนื่องของสมองในส่วนของ basal ganglia ที่เรียกว่า striatum เสียไป (ภาพที่ 2) ส่งผลให้เกิดการทำงานที่ไม่สมดุลย์ในส่วนของ direct และ indirect pathway ใน basal ganglia ทำให้เกิดอาการสั่นและเคลื่อนไหวช้า. อาการส่วนใหญ่จะแสดงให้เห็นชัดเจน เมื่อจำนวนเซลล์ (dopaminergic cells) ในส่วนของ SNc ลดน้อยลงไป เป็นอย่างน้อยร้อยละ 60 จากปกติ อัตราการลดจำนวนของเซลล์ในส่วน SNc ในผู้ป่วยพาร์กินสันก็จะสูงกว่า (ร้อยละ 6-13) คนปกติที่อายุใกล้เคียงกัน (ร้อยละ 2)3 การตรวจทางพยาธิสภาพในสมองของผู้ป่วยโรคพาร์กินสันก็จะ พบว่า substantia nigra ที่ปกติมีสีเข้มค่อนข้างดำ ในคนปกติก็จะจางลงไป การตรวจทางจุลพยาธิสภาพ ก็จะพบ Lewy body (ภาพที่ 3) ซึ่งเป็นก้อนโปรตีน (inclusions) ใน cytoplasm ที่พบมากในเซลล์สมองส่วน SNc, locus coeruleus, thalamus และพบบ้างในส่วนของ cerebral cortex. การพบ Lewy body ไม่ได้บ่งเป็นสิ่งที่ใช้วินิจฉัยโรคพาร์กินสันแต่ ย่างเดียว เนื่องจาก Lewy body สามารถพบได้ ในผู้สูงอายุที่ไม่มีอาการของโรคพาร์กินสัน และโรคเสื่อมทางระบบประสาทอื่นๆ.
การเสื่อมของเซลล์ในส่วน SNc ซึ่งมีหน้าที่ในการผลิต dopamine ส่งผลให้ปริมาณของ dopamine ในสมองมีน้อยลง โดยปกติแล้ว dopamine ถูกเปลี่ยนมาจาก amino acid tyrosine โดยใช้เอนไซม์ที่ชื่อว่า Tyrosine hydroxylase (TH) (ภาพที่ 4). TH นี้ก็มีปริมาณน้อยลงในผู้ป่วย. โรคพาร์กินสันเช่นเดียวกัน หลังจาก dopamine ถูกผลิตขึ้นมาก็จะถูกเปลี่ยนต่อไป โดยเอนไซม์ที่เรียกว่า Monoamine oxidase (MAO) และ Catechol-O-methyl transferase (COMT) จนเป็นสารสุดท้ายที่เรียกว่า Homova nillic acid (HVA) ก่อนที่จะถูกกำจัดออกไปจากร่างกาย เอนไซม์ MAO และ COMT นี้มีความสำคัญเพราะเป็นตำแหน่งของยาที่ใช้ในการรักษาโรคพาร์กินสัน ในปัจจุบัน ออกฤทธิ์โดยการยับยั้งเอนไซม์ดังกล่าว.
อาการของโรคพาร์กินสัน
เนื่องจากโรคพาร์กินสันเกิดมาจากการเสื่อมของสมองในส่วนที่เรียกว่า basal ganglia อาการที่เกิดขึ้นโดยส่วนใหญ่ จะเป็นผลจากการทำงานที่เสียไปในส่วนของ basal ganglia (ที่รวมถึง Caudate, Putamen, Globus pallidus interna (GPi), Globus pallidus externa (GPe), Subthalamic nucleus และ Substantia nigra (SN)) ที่เรียกว่า Extrapyramidal syndromes ซึ่งได้แก่ 1) การเคลื่อนไหว ช้า (bradykinesia) และน้อย (hypokinesia) 2) อาการแข็งเกร็ง (rigidity) 3) อาการสั่น (tre-mor) และ 4) อาการทรงตัวไม่สม่ำเสมอ (postural instability). การวินิจฉัยว่าเป็นโรคพาร์กินสันอย่างแน่นอน (definite Parkinson's disease) สามารถทำได้เมื่ออาการเกิดขึ้นอย่างน้อย 3 ใน 4 อย่างตามที่กล่าวไว้ข้างต้นในผู้ป่วยนั้น หรืออย่างน้อยอาการ 2 ใน 4 อย่างรวมกับอาการอีก 1 อย่าง ที่เกิดขึ้นใน ข้างใดข้างหนึ่งของร่างกาย. Probable Parkinson's disease สามารถวินิจฉัยได้เมื่อมีอาการอย่างน้อย 2 ใน 4 อย่างตามข้างต้น หรืออาการอย่างน้อย 1 อย่างที่เกิดขึ้นเพียงข้างใดข้างหนึ่ง. Possible Parkinson's disease สามารถวินิจฉัยได้เมื่อมีอาการ 1 ใน 4 อย่างดังกล่าว.4 ลักษณะเฉพาะอย่างหนึ่งของโรค พาร์กินสัน คืออาการมักจะเริ่มที่ข้างใดข้างหนึ่งของร่างกายโดยเฉพาะในช่วงแรก. ในปัจจุบันยังเป็นที่ทราบกันว่า ก่อนที่อาการที่กล่าวไว้ข้างต้นจะเกิดขึ้น ผู้ป่วยโรคพาร์กินสันมักจะมีอาการอย่างอื่นมาก่อน (prodromal manifestations) ที่พบได้บ่อยคือ การดมกลิ่น และรับรสอาหารที่ลดน้อยลง อาการเพลีย เป็นต้น ซึ่งสามารถเกิดก่อนอาการทางการเคลื่อนไหวได้นานถึง 6 ปี.
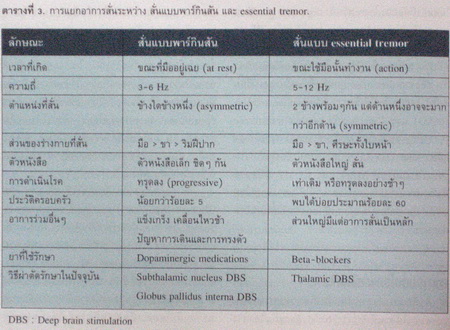
ในอาการทั้ง 4 อย่างที่กล่าวไว้ข้างต้น อาการสั่นเป็นอาการที่พบได้บ่อยที่สุด โดยเป็นอาการแรกในร้อยละ 70 ของผู้ป่วยพาร์กินสันที่มาพบแพทย์. อาการสั่นโดยส่วนใหญ่จะเริ่มที่มือ โดยเฉพาะที่ปลายนิ้ว เป็นในลักษณะที่เรียกว่า Pill rolling tremor. อาการสั่นมักจะเริ่มที่ข้างใดข้างหนึ่งก่อนที่จะเป็นทั้ง 2 ด้านในระยะหลัง นอกเหนือจากนี้ อาการสั่นแบบพาร์กินสันโดยส่วนใหญ่จะเกิดขณะที่มือนั้นอยู่เฉย (rest tremor) ด้วยความถี่ประมาณ 4-7 Hz เช่นขณะที่นั่งดูโทรทัศน์อยู่ เป็นต้น. อาการสั่นจะลดน้อยลงเมื่อผู้ป่วยใช้มือนั้นทำงาน เช่น เขียนหนังสือ หรือตักอาหาร เป็นต้น. อาการสั่นในโรคพาร์กินสัน ก็สามารถเกิดขึ้นได้ในขณะที่ใช้มือนั้นทำงานประมาณร้อยละ 40 แต่มักจะเป็นในระยะหลัง หรือเกิดร่วม กับอาการสั่นขณะที่มือนั้นอยู่เฉย (re-emergent tremor). อาการมือสั่นในขณะเดินโดยส่วนมากเกิดมาจากโรคพาร์กินสัน เช่นเดียวกับอาการสั่นที่คาง และริมฝีปาก ถ้าเป็นมากอาการสั่น สามารถเกิดได้ทั้งมือ และขาทั้ง 2 ด้าน แยกได้ยากจากอาการสั่นแบบ essential tremor (ตารางที่ 3) นอกจากนี้ผู้ป่วยโรคพาร์กินสันมักจะเขียนหนังสือตัวเล็กลง (micrographia) (ภาพที่ 5).
อาการแข็งในโรคพาร์กินสัน (rigidity) โดยส่วนมากจะเกิดที่แขน หรือขาในข้างเดียวกับที่มีอาการสั่น. ผู้ป่วยโดยส่วนใหญ่มักจะไม่บ่นถึงอาการแข็ง เกร็ง แต่อาการนี้มักจะเป็นอาการที่ทำให้เกิดความลำบาก ในผู้ป่วยมากที่สุด. ทำให้เคลื่อนไหวได้ช้า เช่น เดินไปห้องน้ำไม่ทัน ลุกขึ้นยืนได้ยาก พลิกตัวบนเตียงได้ยาก หยิบจับของได้ลำบาก เขียนหนังสือไม่ถนัด เป็นต้น. อาการเหล่านี้มักจะเป็นมากตอนเช้าตรู่ เมื่อตื่นขึ้นมากลางดึก หรือตอนช่วงบ่ายๆ ซึ่งมักจะสอดคล้องกับช่วงที่ระดับยาลดต่ำ อาการแข็งที่ขาสามารถทำให้ผู้ป่วยหกล้มเป็นอันตรายได้. อาการแข็งในโรคพาร์กินสัน จะเป็นในลักษณะของ rigidity ซึ่งเป็นอาการแข็งที่สามารถตรวจพบได้ตลอด เช่น ขณะที่แพทย์ยืดแขนขาผู้ป่วย ไม่ขึ้นกับความเร็วของการกระทำ. ในทางกลับกัน อาการแข็งในลักษณะของ spasticity ซึ่งเกิดในโรคของ pyramidal system จะเป็นอาการแข็งเกร็งที่เปลี่ยนไปกับความเร็วของการยืดแขนและขาผู้ป่วย.
อาการเคลื่อนไหวช้า และเล็ก (bradykinesia and hypokinesia) มักจะเริ่มที่มือ หรือส่วนของร่างกายที่มีอาการสั่น อาการช้าในผู้ป่วยจะเป็นทั้งการเริ่มที่ช้า รวมกับการเคลื่อนไหวที่ช้า ส่วนหนึ่งอาจเป็นผลของอาการแข็ง เกร็งของแขนและขาในส่วนนั้น. อาการช้าที่เป็นอย่างมาก อาจส่งผลให้ผู้ป่วยนั้นไม่สามารถขยับแขนขาข้างนั้น หรือทั้งตัวได้เลย หรือที่เรียกว่า akinesia.
ผู้ป่วยโรคพาร์กินสันมีลักษณะการเดินที่เฉพาะหลายอย่าง และสามารถสังเกตได้ง่าย ถ้าได้เคยเห็นมาก่อน อย่างแรก ผู้ป่วยพาร์กินสันมักจะเดินซอยเท้าถี่ และเล็ก (shuffle) ในลักษณะที่โน้มตัวไปข้างหน้า (festination) ในบางครั้งผู้ป่วยจะเดินย่ำเท้าอยู่กับที่เหมือนกับเท้าติดอยู่กับพื้น (gait freezing) แต่ถ้าวางเส้น หรือปากกาบนพื้นข้างหน้าผู้ป่วยที่เดินติด (visual cues) จะทำให้ผู้ป่วยนั้นก้าวเท้าออกได้ ซึ่งเป็นลักษณะเฉพาะอย่างหนึ่งของการเดินในโรคพาร์กินสัน. ผู้ป่วยโรคพาร์กินสันมักจะเดินไม่แกว่งแขน โดยเฉพาะในด้านที่มีอาการมาก คอและศีรษะ ก้ม (stoop) ซึ่งในบางครั้งสามารถเป็นมากจนโน้มลงมาเกือบครึ่งตัว หรือที่เรียกว่า camptocormia เมื่อกลับตัวขณะเดิน ผู้ป่วยมักจะกลับทั้งตัวไปพร้อมๆ กัน ร่วมกับซอยเท้าถี่ๆ (En bloc turn). ปัญหาการเดินในลักษณะที่กล่าวนี้เป็นสาเหตุสำคัญอย่างหนึ่ง ที่ทำให้ผู้ป่วยพาร์กินสันหกล้มได้. การตรวจการทรงตัวในผู้ป่วยพาร์กินสัน โดยใช้วิธีที่เรียกว่า pull test สามารถทำได้โดยยืนอยู่ข้างหลังผู้ป่วย และใช้มือพลักผู้ป่วยให้ถอยหลัง ผู้ป่วยที่ไม่มีปัญหาการทรงตัวจะไม่ล้ม และสามารถก้าวถอยเพื่อทรงตัวได้ ในขณะที่ผู้ป่วยพาร์กินสันที่มีปัญหาในเรื่องการทรงตัว จะถอยหลังถี่ๆ หลายก้าว ก่อนที่จะทรงตัวได้ หรืออาจจะตัวเอนมาข้างหลัง ล้มได้ถ้าไม่ถูกพยุงไว้.
นอกเหนือจากอาการเด่นทางการเคลื่อนไหวที่ได้กล่าวไว้ข้างต้น ผู้ป่วยโรคพาร์กินสันสามารถมีอาการที่ครอบคลุมไปถึงระบบอื่นๆ แต่อาการเหล่านี้อาจจะไม่เด่นชัด หรือได้รับการสนใจจากแพทย์น้อย หรือที่เรียกว่า nonmotor manifestations ซึ่งสามารถเกิดอาการได้กับแทบทุกระบบ5 ดังเช่น ในระบบทางเดินอาหารที่แสดงออกในลักษณะของอาการท้องผูก เนื่องจากการเคลื่อนไหวของระบบทางเดินอาหารที่ช้าลง. ในระบบประสาทแบบ autonomic เช่น ปัญหาในการขับปัสสาวะ อาการเสื่อมสมรรถนะทางเพศ ปัญหาเรื่องความดันโลหิตที่ต่ำลงเมื่อเปลี่ยนจากท่านอน นั่ง มาเป็นการยืน (postural hypotension) อาการหลงลืม (dementia) ในโรคพาร์กินสัน มักจะเป็นในลักษณะของ subcortical dementia แต่โรคอัลไซเมอร์ก็สามารถเกิดในผู้ป่วยพาร์กินสันได้. ในระบบจิตเวช เช่น อาการซึมเศร้า ซึ่งสามารถเกิดได้ร่วมกับโรคพาร์กินสันเอง หรือเกิดเนื่องจากความรู้สึกของผู้ป่วยที่ได้รับทราบว่าตนเองเป็นโรคทางระบบประสาท (reactive depression) อาการวิตกกังวล (anxiety) ซึ่งพบได้บ่อยเช่นเดียวกัน และไม่มีความสอดคล้องกับความรุนแรงของโรค หรือยาที่ใช้รักษาอาการเห็นภาพหลอน (visual hallucinations) ซึ่งมักจะเป็นตอนบ่ายหรือตอนกลางคืน และเกี่ยวข้องกับยา dopaminergic therapy ที่ได้รับ. ผู้ป่วยโรคพาร์กินสันที่เห็นภาพหลอน ส่วนมากจะรู้ตัวว่าภาพที่เห็นนั้นไม่จริง และมักจะเห็นเป็นในลักษณะของคน หรือต้นไม้ในมุมห้อง ไม่ใช่ภาพหลอนที่น่ากลัว. ปัญหาในเรื่องของการนอนก็สามารถเกิดขึ้นได้เช่นเดียวกัน ซึ่งส่วนมากจะเป็นในลักษณะของ sleep fragmentation คือ นอนหลับไปแล้วแต่ตื่นขึ้นมากลางดึก และไม่สามารถกลับไปนอนได้. ต่างจากปัญหาในเรื่องของการเริ่มหลับ (initial insomnia) ซึ่งพบได้น้อยกว่าในโรคพาร์กินสัน REM sleep behavior (REM) disorders สามารถเกิดได้เช่นเดียวกัน โดยส่วนมากผู้ดูแลผู้ป่วยจะเป็นผู้ ให้ประวัติว่าเหมือนผู้ป่วยตื่นขึ้นมาเอะอะ โวยวายกลางดึก โดยที่ผู้ป่วยไม่รู้ตัว. อาการปวด (pain) เป็นอาการที่พบมากถึงร้อยละ 46 ในผู้ป่วยพาร์กินสัน และมีได้หลายสาเหตุ ทั้งที่เกิดเนื่องจากอาการแข็งเกร็งแบบ rigidity ตามแขนขา หรืออาการปวดท้อง ปวดบริเวณใบหน้า หรือปวดตามลำตัวโดยไม่มีลักษณะเฉพาะ ซึ่งสาเหตุของอาการปวดเหล่านั้นไม่เป็นที่ทราบแน่นอน.
Young-onset Parkinson's disease (YOPD)
Young-onset Parkinson's disease หมายถึง ผู้ป่วยโรคพาร์กินสันที่มีอาการแรกเริ่ม เมื่ออายุน้อยกว่า 40 ปี อาการเริ่มต้นคล้ายเคียงกับอาการของผู้ป่วยโรคพาร์กินสันโดยทั่วไป แต่การวินิจฉัยผู้ป่วยในกลุ่มนี้จะค่อนข้างช้า เนื่องจากแพทย์หลายท่านยังมีความเข้าใจว่า ผู้ป่วยพาร์กินสันควรจะมีอายุที่มากกว่า 50-60 ปี และการนึกถึงโรคพาร์กินสัน ในผู้ป่วยที่อายุน้อยกว่า 40 ปียังมีน้อย. ลักษณะทางพยาธิวิทยาในผู้ป่วย YOPD จะเหมือนกับผู้ป่วยโรคพาร์กินสันโดยทั่วไป หากแต่การดำเนินโรค (natural history) จะมีความแตกต่าง. โดยทั่วไปผู้ป่วย YOPD จะมีปัญหาในเรื่องของ cognitive dysfunction ที่น้อยกว่า ร่วมกับปัญหาการเดิน และปัญหาที่เป็น nonmotor manifestations ที่น้อยกว่าผู้ป่วยพาร์กินสันที่อายุมาก แต่ผู้ป่วย YOPD มักจะมีปัญหาหลักในเรื่องการตอบสนองต่อยา dopaminergic ที่ไม่สม่ำเสมอ (motor fluctuations) เมื่อมีการดำเนินโรคไปในระยะหนึ่ง โดยเฉพาะในช่วง 2 ปีแรกซึ่งนับว่าเกิดค่อนข้างเร็วถ้าเทียบกับกลุ่มผู้ป่วยพาร์กินสันปกติ. ดังนั้นหลักการรักษาด้วยยาในกลุ่ม dopa minergic ในผู้ป่วย YOPD จะมีความสำคัญ (รายละเอียดอยู่ในบทของการรักษา) เพื่อต้องการที่จะให้ปัญหาในการตอบสนองต่อยาที่ไม่สม่ำเสมอ เกิดช้าที่สุด.
Juvenile parkinsonism (JP)
JP หมายถึง อาการพาร์กินโซนิซึมที่เกิดใน ผู้ป่วยอายุก่อน 21 ปี เพราะฉะนั้น JP จะรวมถึงกลุ่มโรคที่ทำให้เกิดอาการพาร์กินโซนิซึมในคนอายุน้อย (ซึ่งต่างจาก PD และ YOPD) ซึ่งมีสาเหตุได้หลายอย่าง6 ดังเช่น โรคทางพันธุกรรมที่เกิดจาก parkin mutations (Autosomal recessive juvenile parkinsonism, ARJP) โรควิลสัน (Wilson's di-sease) Dopa-responsive dystonia (DRD) และอื่นๆ.
ลักษณะอาการพาร์กินโซนิซึมใน JP อาจจะไม่แตกต่างจากโรคพาร์กินสัน ซึ่งในบางครั้งอาจไม่สามารถแยกจากโรคพาร์กินสันได้ หากแต่ว่าเกิดในผู้ป่วยที่อายุน้อยกว่า. ผู้ป่วย JP ในบางกลุ่มโดยเฉพาะ ARJP สามารถตอบสนองต่อ levodopa ได้ดีคล้ายกับผู้ป่วยพาร์กินสัน แต่ปัญหาในเรื่องของการตอบสนองต่อยาไม่สม่ำเสมอ หรือที่เรียกว่า motor complications สามารถเกิดได้เร็วกว่าผู้ป่วยพาร์กินสันทั่วไป และมีอาการของดีสโทเนีย (dystonia) ที่เด่นชัดกว่า.
เนื่องจาก JP สามารถมีสาเหตุได้จากหลายโรค ดังนั้นพยาธิวิทยาจึงมีความแตกต่างกันไปขึ้นอยู่กับสาเหตุนั้น โดยทั่วไป neuronal loss และ gliosis เกิดขึ้นในส่วนของ substantia nigra ในส่วนของ ARJP ที่เกิดจาก parkin mutation ถึงแม้ว่าผู้ป่วยจะมีลักษณะอาการคล้ายผู้ป่วยพาร์กินสันดังที่ได้กล่าวไว้ข้างต้น แต่พยาธิวิทยามักไม่ปรากฏ Lewy body ในส่วนของ substantia nigra หรือสมอง ส่วนอื่นๆ.
Essential tremor (ET)
ถึงแม้ว่าโรค essential tremor ไม่ได้ถูกจัดไว้เป็นสาเหตุของกลุ่มอาการพาร์กินโซนิซึม เนื่องจากมีอาการหลักเป็นอาการสั่นเพียงอย่างเดียว แต่จะขอกล่าวถึงไว้ในบทความนี้ เนื่องจากผู้ป่วยโรคพาร์ กินสันในระยะแรก มักจะมีอาการสั่นเป็นอาการหลัก ซึ่งสามารถทำให้เกิดการสับสนระหว่างการวินิจฉัยแยกโรคระหว่างโรคสั่นแบบพาร์กินสัน หรือสั่นแบบ essential tremor.
ถ้าเราเข้าใจถึงลักษณะอาการสั่นของทั้ง 2 โรคเป็นอย่างดี การแยกระหว่างสั่นแบบพาร์กินสัน หรือ ET มักจะไม่ยาก แต่ต้องอาศัยการสังเกตที่ละเอียด และประวัติจากผู้ป่วยย้อนหลัง อย่างที่ได้กล่าวไว้ข้างต้น. อาการสั่นของโรคพาร์กินสันจะเริ่มด้านใดด้านหนึ่งก่อนในขณะที่มือหรือขาอยู่เฉยๆ (asymmetric rest tremor) ซึ่งต่างจากอาการสั่นในโรค ET ซึ่งมักจะเป็นพร้อมกันทั้ง 2 ข้าง. แต่ผู้ป่วยอาจสังเกตว่า อาการสั่นมีมากกว่าด้านใดด้านหนึ่ง นอกเหนือจากนั้น อาการสั่นในโรค ET จะเป็นขณะที่ใช้มือนั้น ทำงาน หรือกิจวัตร (symmetric action tremor). ประวัติที่แพทย์มักได้จากผู้ป่วย คือ อาการสั่นเกิดขึ้น ขณะใช้มือนั้นหยิบแก้วน้ำ หรือใช้ช้อนกินอาหารซึ่งเป็นกิจวัตรประจำวันที่ถูกกระทบกระเทือนในโรค ET มากที่สุด ในขณะที่ผู้ป่วยโรคพาร์กินสันเขียนตัวหนังสือเล็กลง ผู้ป่วยโรค ET จะเขียนตัวหนังสือที่ใหญ่ขึ้นและสั่น. การสังเกตลายมือนั้น เป็นวิธีที่ผู้เขียนใช้บ่อยในการตรวจผู้ป่วยสั่น เพื่อแยกระหว่าง ทั้ง 2 โรค. เมื่อผู้ป่วยพาร์กินสันมีอาการนานขึ้น การแยกโรค ET ออกจากโรคพาร์กินสันอาจจะง่ายขึ้น เนื่องจากผู้ป่วยโรค ET ยังคงมีแต่อาการสั่น ในขณะที่ผู้ป่วยโรคพาร์กินสันจะมีอาการพาร์กินโซนิซึมอื่นๆ เพิ่มเติม ดังเช่นในเรื่องการเคลื่อนๆ ไหวช้า แข็งและเดินลำบากเพิ่มเติม ลักษณะอาการที่แตกต่าง อื่นๆ ได้สรุปไว้ดังตารางที่ 3.
การวินิจฉัยแยกอาการสั่นระหว่างโรคพาร์กินสัน และ ET ให้ถูกต้องแต่แรกเริ่มมีความสำคัญเป็นอย่างยิ่ง เนื่องจากการดำเนินโรค และการรักษาที่แตกต่างกันอย่างชัดเจนระหว่างทั้ง 2 โรค. ยาที่ใช้ในการรักษาโรค ET โดยส่วนใหญ่จะใช้ nonselective beta-blocker ดังเช่น propranolol เป็นยาหลัก (first-line therapy) ในขณะที่ยาที่ใช้ในการรักษาโรคพาร์กินสัน โดยส่วนใหญ่จะอยู่ในกลุ่มของ dopa minergic medications.
Drug-induced parkinsonism
ประวัติจากผู้ป่วยหรือญาติเป็นสิ่งที่สำคัญที่สุด เมื่อแพทย์สงสัยว่าอาการพาร์กินโซนิซึมนั้น อาจเกิดขึ้นจากยา. โดยส่วนใหญ่ยาที่ทำให้เกิดอาการพาร์กินโซนิซึม มักจะเป็นยาที่ไปจับและยับยั้งการทำงานของ dopamine receptors ซึ่งส่วนใหญ่จะเป็นยาในกลุ่มของจิตเวช โดยเฉพาะในกลุ่ม neuroleptics และยารักษาอาการคลื่นไส้อาเจียนบางชนิด ยกตัวอย่างเช่น metoclopramide. นอกจากนี้ยังมียาอีกหลายชนิด ที่สามารถทำให้เกิดอาการพาร์กินโซนิซึมได้ ดังเช่น sodium valproate ซึ่งใช้ระงับอาการชัก หรือยาทางโรคหัวใจ และความดันโลหิตสูงบางชนิด ดังเช่น amiodarone หรือ nifedipine เป็นต้น. ยาอื่นๆ ที่สามารถทำให้เกิดอาการพาร์กินโซนิซึม ได้รวบรวมไว้ในตารางที่ 4.

ในบางครั้งอาการพาร์กินโซนิซึมที่เกิดจากยา อาจไม่สามารถแยกออกได้จากโรคพาร์กินสัน โดยเฉพาะในบางครั้งที่ประวัติยาไม่ชัดเจน อาจทำให้การวินิจฉัยแยกโรคเป็นไปได้ลำบาก. แต่โดยส่วน มากโรคพาร์กินสันมักจะเริ่มขึ้นด้านใดด้านหนึ่ง ใน ขณะที่อาการพาร์กินโซนิซึมจากยามักจะเป็น 2 ข้างพร้อมๆ กัน. อาการสั่นที่เกิดจากยา มักจะเป็นในขณะที่ใช้มือนั้นทำงาน โดยมีความถี่สูงและสั่นน้อยๆ ไม่ค่อยชัด (fine amplitude bilateral action tremor) ซึ่งต่างจากอาการสั่นของโรคพาร์กินสันที่ เป็นด้านใดด้านหนึ่งขณะมืออยู่เฉย ในลักษณะคล้ายจับเม็ดยา (Pill-rolling asymmetric rest tremor).7
ถ้าการแยกโรคไม่สามารถทำได้เมื่อผู้ป่วยมาหาแพทย์เป็นครั้งแรก แพทย์อาจต้องอาศัยการสังเกต อาการที่ต่อเนื่อง เพื่อช่วยในการแยกวินิจฉัยโรคพร้อมกับหยุดยาที่อาจทำให้เกิดอาการพาร์กินโซนิซึม. ถ้าเป็นไปได้ (ในบางครั้งอาจไม่สามารถหยุดยาได้ โดยเฉพาะในกลุ่ม neuroleptics) ในผู้ป่วยพาร์กินโซนิซึมที่เกิดจากยา เมื่อหยุดยาแล้วมักมีอาการที่ดีขึ้น อาการพาร์กินโซนิซึมมักลดน้อยลง แต่อาจไม่หายสนิทภายใน 2-4 สัปดาห์หรืออาจมากกว่า. ในผู้ป่วยบางกลุ่มที่ใช้ยา typical neuroleptics อย่าง ต่อเนื่อง ดังเช่น haloperidol หรือ chlorpromazine แพทย์อาจพิจารณาเปลี่ยนยาเป็นในกลุ่ม atypical neuroleptics ดังเช่น quetiapine, olanzapine หรือ clozapine เป็นต้น ถ้ายังมีความจำเป็นที่ต้องใช้ neuroleptics ในผู้ป่วยท่านนั้นอยู่ เนื่องจาก atypical neuroleptics จะทำให้เกิดอาการพาร์กินโซนิซึมน้อยกว่า. อย่างไรก็ตาม ในปัจจุบันยังไม่มีคำแนะนำที่แน่นอน (practice guidelines) เมื่อกรณีเช่นนี้เกิดขึ้น ซึ่งการตัดสินใจในแต่ละรายอาจมีความแตกต่างกันไป ขึ้นอยู่กับแพทย์ผู้รักษา และอาการผู้ป่วยโดยรวมในขณะนั้น.
Vascular pseudoparkinsonism
โรคในกลุ่มนี้ มีชื่อเรียกหลายชื่อ ดังเช่น multi-infarct parkinsonism หรือ arteriosclerotic parkinsonism ซึ่งสาเหตุของอาการพาร์กินโซนิซึมก็เป็นไปตามชื่อของโรค คือเกิดเนื่องจากหลอดเลือดขนาดเล็กที่มีการอุดตัน ประวัติของผู้ป่วยมักจะเด่นชัดในเรื่องของปัจจัยเสี่ยงของโรคหลอดเลือด (vascular risk factors) ดังเช่นโรคความดันโลหิตสูง โรคเบาหวาน เป็นต้น ร่วมกับอาการที่ค่อยๆ ทรุดลงเป็นช่วงๆ (step-wise deterioration) อาการพาร์กินโซนิซึมมักจะเด่นที่ขาทั้ง 2 ข้างเท่าๆ กัน หรือที่เรียกกันว่า lower body parkinsonism.8 นอกจากนี้ แพทย์ควรตรวจพบความผิดปกติทางระบบประสาทจากการตรวจร่างกายที่นอกเหนือจากอาการพาร์-กินโซนิซึม (focal neurological signs) ดังเช่น อาการอ่อนแรงด้านใดด้านหนึ่ง (hemiparesis). การ ศึกษาทางรังสีวิทยา ไม่ว่าจะเป็น CT หรือ MRI ของระบบประสาท ควรบ่งชี้ถึงปัญหาของหลอดเลือดขนาดเล็ก (ภาพที่ 6) ซึ่งรอยโรคมักจะอยู่ใน white matter หรือ deep gray nuclei ดังเช่น ในส่วนของ basal ganglia หรือรอบๆ โพรงสมอง (ventricles) เป็นต้น.
อาการ Lower body parkinsonism มักแสดงออกให้เห็นชัดในเรื่องของการเดิน ดังนั้นผู้ป่วยในกลุ่มนี้ อาจมีปัญหาในเรื่องของการเดินติด หรือเริ่มเดินออกได้ลำบาก (gait freezing or hesitation) นอกเหนือจากนี้ ก้าวเดินจะสั้น และแยกออกทางด้านข้าง (wide-based Shuffle gait). ปัญหาในการทรงตัวมักจะเกิดขึ้น เมื่อผู้ป่วยต้องเลี้ยว หรือหันหลังกลับ ทำให้เกิดการล้ม ประสบอุบัติเหตุได้ง่าย. ผู้ป่วย vascular pseudoparkinsonism มักจะไม่มีอาการสั่น หรือถ้ามีก็น้อย ต่างจากผู้ป่วยโรคพาร์กินสัน. การตรวจร่างกายอื่นๆ อาจพบลักษณะของ vascular dementia หรือปัญหาในเรื่องของการควบคุมปัสสาวะร่วมด้วย.
รุ่งโรจน์ พิทยศิริ พ.บ., M.R.C.P.(UK.)
American Board of Psychiatry & Neurology
ผู้ช่วยศาสตราจารย์, ศูนย์รักษาโรคพาร์กินสันและกลุ่มโรคความเคลื่อนไหวผิดปกติ,
สาขาวิชาประสาทวิทยา, คณะแพทยศาสตร์, จุฬาลงกรณ์มหาวิทยาลัย
- อ่าน 24,821 ครั้ง
 พิมพ์หน้านี้
พิมพ์หน้านี้




