โอกาสที่จะติดเชื้อไวรัสบี (HBV) ขึ้นกับ degree ของการสัมผัสกับเลือด และ HBeAg status ของผู้ป่วยที่เป็นเจ้าของเลือด โอกาสการเกิด serologic evidence ของการติดเชื้อ HBV จะประมาณร้อยละ 37-62 และโอกาสเกิด clinical hepatitis ประมาณร้อยละ 22-31 หลังถูกเข็มแทง ในกรณีที่เลือดนั้นมาจากผู้ป่วยที่มี HBeAg เป็นบวก ในขณะที่โอกาสเกิด serologic evidence ของการติดเชื้อ HBV จะประมาณร้อยละ 23-37 และโอกาสเกิด clinical hepatitis จะเพียงประมาณร้อยละ 1-6 ถ้าเลือดนั้นมาจากผู้ป่วยที่มี HBeAg เป็นลบ.1,2
การศึกษาให้ HBIG ร่วมกับวัคซีนป้องกันตับอักเสบบี ในเด็กแรกเกิดจากมารดาที่มี HBeAg เป็นบวก สามารถป้องกันการติดเชื้อไวรัสบีได้ถึงร้อยละ 85-953,4 ในขณะที่การให้ multiple dose ของ HBIG อย่างเดียว หรือฉีดวัคซีนป้องกันไวรัสบีเพียงอย่างเดียว 3 เข็ม จะป้องกันการติดเชื้อไวรัสบีได้ร้อยละ 70-755 ในการศึกษาให้ multiple dose ของ HBIG โดยเริ่มฉีดเข็มแรกภายใน 1 สัปดาห์ หลังถูกเข็มตำในบุคลากรทางการแพทย์พบว่าสามารถป้องกันการติดเชื้อไวรัสบีได้ร้อยละ 756-8 ดังนั้นจึงแนะให้ฉีด HBIG ร่วมกับวัคซีนป้องกันไวรัสบี ในบุคลากรที่สัมผัสกับไวรัสบี (percutaneous หรือ mucous exposure)
การศึกษาผลข้างเคียงของวัคซีนป้องกันไวรัสบีในเด็กแรกเกิด เด็ก และผู้ใหญ่ พบว่าปลอดภัย9,10 ผลข้างเคียงที่พบได้บ่อยคือ ปวดบริเวณตำแหน่ง ที่ฉีด ไข้ต่ำๆ10-15 โอกาสเกิดแพ้แบบ anaphylaxis พบได้ 1 ใน 600,000 แม้ว่าจะมีรายงานผู้ป่วย multiple sclerosis, optic neuritis, rheumatoid arthritis และ Guillain-Barre Syndrome ในผู้ป่วยหลังฉีดวัคซีนไวรัสบี16-18 แต่ในการศึกษาขนาดใหญ่และเปรียบเทียบกับประชากรที่ไม่ได้ฉีดวัคซีนในไต้หวัน นิวซีแลนด์ และ อเมริกา พบว่าไม่มีความสัมพันธ์ของ การฉีดวัคซีนป้องกันไวรัสบีกับการเกิดโรคดังกล่าว19,20
ผลข้างเคียงจาก HBIG นั้นพบได้น้อยมาก เท่าที่มีรายงานคือ ปวดบริเวณตำแหน่งที่ฉีดลมพิษ angioedema และ anaphylaxis21
ไม่มีหลักฐานผลข้างเคียงในหญิงตั้งครรภ์และทารกในครรภ์ ดังนั้น ไม่มีข้อห้ามในการฉีด HBIG และ วัคซีนป้องกันไวรัสบีในหญิงตั้งครรภ์
Recommendation 1
บุคลากรที่ทำงานที่มีโอกาสสัมผัสกับเลือด, blood- contaminated body fluid, น้ำเหลือง, body fluids หรืออุปกรณ์ที่แหลมคม ควรได้รับการฉีดวัคซีนป้องกันไวรัสบี22, 23 เนื่องจากความชุกของการ ติดเชื้อไวรัสบีเรื้อรังในประเทศไทยสูง ดังนั้นควรเจาะเลือดตรวจดูก่อนว่าเคยได้รับเชื้อไวรัสบีแล้วหรือยัง โดยการตรวจ anti-HBc ถ้ามี anti-HBc เป็นลบ จึงพิจารณาฉีดวัคซีน โดยฉีดเข้าชั้นกล้ามเนื้อ ครบ 3 เข็ม ที่ 0, 1 และ 6 เดือน
Recommendation 2
ในบุคลากรที่มีปัจจัยเสี่ยงต่อเลือด และ/หรือ percutaneous injury ควรมีการตรวจ anti HBs 1-2 เดือนหลังฉีดวัคซีนป้องกันไวรัสบีครบเข็มที่ 323 ในกรณีที่ anti-HBs <10 mIU/mL ควรพิจารณาสาเหตุเช่น มี HBsAg เป็นบวกหรือไม่ ในกรณีมี HBsAg เป็นลบ ควรได้รับการฉีดวัคซีนป้องกันไวรัสบีอีก 3 เข็มที่ 0,1 และ 6 เดือน24
Recommendation 3
ควรทำความสะอาดด้วยสบู่และน้ำบริเวณบาดแผลหรือผิวหนังที่สัมผัสกับเลือดหรือ body fluids จากผู้ป่วยที่ติดเชื้อไวรัสบี และควรชำระด้วยน้ำ (flush) ในบริเวณเยื่อบุ (mucous membrane) และควรแจ้งรายงานให้หน่วยงานที่รับผิดชอบทราบ
Recommendation 4
การให้ HBIG และ HBV vaccine จะขึ้นอยู่กับว่าบุคลากรที่สัมผัส เคยฉีดวัคซีนป้องกันไวรัสบีและมีการตอบสนองต่อการฉีดอย่างไร และภาวะของผู้ป่วยที่เป็นแหล่งของเลือดหรือ body fluids ดังแสดงไว้ในตารางที่ 1
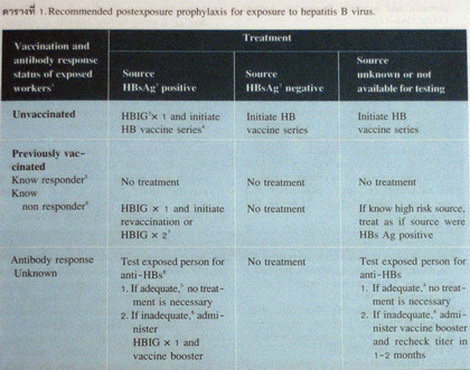
1Persons who have previously been infected with HBV are immune to reinfection and do not require postexposure prophylaxis.
2Hepatitis B surface antigen.
3Hepatitis B immune globulin; dose is 0.06 mL/kg intramuscularly.
4Hepatitis B vaccine.
5A responder is a person with adequate levels of serum antibody to HBsAg (i.e., anti-HBs >10 mIU/mL).
6A nonresponder is a person with inadequate response to vaccination (i.e, serum anti-HBs <10 mIU/mL).
7The option of giving one dose of HBIG and reinitiating the vaccine series is preferred for nonresponders who have not completed a second 3-dose vaccine series. For persons who previously completed a second vaccine series but failed to respond, two doses of HBIG are preferred.
8Antibody to HBsAg.
ธีระ พิรัชวิสุทธิ์ พ.บ.
รองศาสตราจารย์ ภาควิชาอายุรศาสตร์
คณะแพทย์ศาสตร์ มหาวิทยาลัยสงขลานครินทร์
เอกสารอ้างอิง
1. Mast EE, Alter MJ. Prevention of hepatitis B virus infection among health-care workers. In : Ellis RW, ed. Hepatitis B vaccines in clinical practice. New York, NY : Marcel Dekker, 1993:295-307.
2. Werner BG, Grady GF. Accidental hepatitis-B-surface-antigen-positive inoculations : of e antigen to estimate infectivity. Ann lntern Med 1982;97:367-9.
3. Beasley RP, Hwang LY, Lee GC, et al. Prevention of perinatally transmitted hepatitis B virus infections with hepatitis B immune globulin and hepatitis B vaccine. Lancet 1993;2:1099-102.
4. Stevens CE, Toy PT, Tong MJ, et al. Perinatal hepatitis B virus transmission in the United States : prevention by passive-active immu-nization. JAMA 1985;253:1740-5.
5. Beasley RP, Hwang LY Stevens CE, et al. Efficacy of hepatitis B immune globulin for prevention of perinatal transmission of the hepatitis B virus carrier state : final report of a randomized double-blind, placebo-controlled trial. Hepatology 1983;3:135-41.
6. Grady GF, Lee VA Prince AM, et al. Hepatitis B immune globulin for accidental exposures among medical personnel : final report of a multicenter controlled trial. J lnfect Dis 1978;138:625-38.
7. Seeff LB, Zimmerman HJ, Wright EC, et al. A randomized double-blind controlled trial of the efficacy of immune serum globulin for the prevention of post-transfusion hepatitis : a Veterans Administration cooperative study. Gastroenterology 1977;72:111-21.
8. Prince AM, Szmuness W, Mann MK, et al. Hepatitis B "immune" globulin : effectiveness in prevention of dialysis-associated hepatitis. N Engl J Med 1975;293:1063-7.
9. CDC. Hepatitis B virus : a comprehensive strategy for eliminating transmission in the United States through universal childhood vaccination : recommendations of the lm-munization Practices Advisory Committee (ACIP). MMWR 1991;40(No. RR-13).
10. Greenberg DP. Pediatric experience with recombinant hepatitis B vaccines and relevant safety and immunogenicity studies. Pediatr Inf Dis J 1993;12:438-45.
11. Szmuness W, Stevens CE, Harley EJ, et al. Hepatitis B vaccine : demonstration of effi- cacy in a controlled clinical trial in a high- risk population in the United States. N Engl J Med 1980;303:833-41.
12. Francis DP, Hadler SC, Thompson SE, et al. The prevention of hepatitis B with vaccine : report of the Centers for Disease Control mul-ti-center efficacy trial among homosexual- men. Ann Intern Med 1982;97:362-6.
13. Stevens CE, Alter HJ, Taylor PE, et al. Hepa-titis B vaccine in patients receiving hemodia-lysis : immunogenicity and efficacy. N Engl J Med 1984;311:495-501.
14. Andre FE. Summary of safety and efficacy data on a yeast-derived hepatiis B vaccine. Am J Med 1989;87(suppl 3A):14S-20S.
15. Zajac BA, West DJ, McAleer WJ, Scolnick EM. Overview of clinical studies with hepatitis B vaccine made by recombinant DNA. J lnfect 1986;13 (suppl A):39-45.
16. Shaw FE, Graham DJ, Guess HA, et al. Postmarketing surveillance for neurologic adverse events reported after hepatitis B vac-cination : experience of the first three years. Am J Epidemiol 1988;127:337-52.
17. Ribera EF, Dutka AJ. Polyneuropathy asso-ciated with administration of hepatitis B vaccine[Letter]. N Engl J Med 1983;309: 614-5.
18. Grotto I, Mandel Y, Ephros M, Ashkenazi I, Shemer J. Major adverse reactions to yeast- derived hepatitis B vaccines-a review. Vaccine 1998:16:329-34.
19. Chen DS. Control of hepatitis B in Asia : mass immunization program in Taiwan. In : Hollinger FB, Lemon SM, Margolis HS, eds. Viral hepatitis and liver disease. Baltimore, MD : Williams and Wilkins, 1991:716-9.
20. Niu MT, Rhodes P, Salive M, et al. Comparative safety of two recombinant hepatitis B vaccines in children : data from the Vaccine Adverse Event Reporting System (VAERS) and Vaccine Safety Datalink (VSD). J Clin Epidemiol 1998;51:503-10.
21. Ellis EF, Henney CS. Adverse reactions following administration of human gamma globulin. J Allerg 1969;43:45-54.
22. Department of Labor, Occupation Safety and Health Administration. 29 CFR Part 1910.1030. Occupational exposure to bloodborne patho-gens; final rule. Federal Register 1991;56: 64004-182.
23. CDC. Immunization of health-care workers : recommendations of the Advisory Committee on Immunization Practices [ACIP] and the Hospital Infection Control Practices Advisory Committee [HICPAC]. MMWR 1997:46 [No. RR-18].
24. Hadler SC, Francis DP, Maynard JE, et al. Long-term immunogenicity and efficacy of hepatitis B vaccine in homosexual men. N Engl J Med 1986;315:209-14[No. RR-4]: 1-17.
- อ่าน 6,203 ครั้ง
 พิมพ์หน้านี้
พิมพ์หน้านี้




