Pulmonary embolism เป็นภาวะหนึ่งที่มีความสำคัญทางคลินิก เนื่องจากมีอาการแสดงที่หลากหลายและคล้ายคลึงกับอีกหลายภาวะ ซึ่งถ้าหากแพทย์ไม่ได้สงสัยหรือให้การวินิจฉัยอย่างถูกต้อง รวมทั้งให้การรักษาอย่างเร่งด่วนอาจเกิดอันตรายถึงชีวิตได้. ดังนั้นจึงควรเข้าใจถึงลักษณะทางคลินิกและแนวทางการดูแลรักษาผู้ป่วยกลุ่มนี้ เพื่อให้การดูแลรักษาเป็นไปอย่างมีประสิทธิภาพยิ่งขึ้น.
อุบัติการณ์การเกิด venous thromboembolism (pulmonary embolism และ deep vein thrombosis) จะพบบ่อยในประชากรทางแถบซีกโลกตะวันตกมากกว่าทางซีกโลกตะวันออก และมีอัตราการเสียชีวิตได้ตั้งแต่ร้อยละ 2.5 จนถึงร้อยละ 28 ขึ้นกับความรุนแรงของโรคและโรคที่พบร่วมด้วย.1,2
ปัจจัยเสี่ยงต่อการเกิด venous thromboembolism
ปัจจัยเสี่ยงที่มีผลต่อการเกิดภาวะ venous thromboembolism มีได้ทั้งจากปัจจัยทางสภาพแวดล้อม, ปัจจัยทางธรรมชาติ, และปัจจัยทางร่างกาย เช่น ฮอร์โมน เป็นต้น. ตัวอย่างของปัจจัยเสี่ยงที่สำคัญ เช่น
1. ความอ้วน มีความสัมพันธ์กับค่า body mass index (BMI) เป็นหลัก โดยมีการศึกษาพบว่าในกลุ่มที่มีค่า BMI ระหว่าง 25-28.9 กก./ตร.ม. และค่าสูงกว่า 29 กก./ตร.ม. มีโอกาสเกิด pulmonary embolism ได้ 1.7 เท่า และ 3.2 เท่าตาม ลำดับเมื่อเทียบกับผู้มีน้ำหนักปกติ.3
2. ปัจจัยทางสุขภาพในเพศหญิง (Women' s health) ได้แก่
=การใช้ยาคุมกำเนิดชนิดกิน พบว่าเพิ่มความเสี่ยงต่อการเกิด pulmonary embolism ทั้งชนิดที่มีปริมาณของเอสโตรเจนมากกว่าหรือน้อยกว่า 50 ไมโครกรัม,หรือชนิดที่มีฮอร์โมนโปรเจสโตเจนกลุ่ม
ใหม่ก็ตาม โดยความเสี่ยงจะยิ่งมากขึ้นในผู้ป่วยกลุ่มที่มีอายุมากและสูบบุหรี่ร่วมด้วย และถ้าหากผู้ป่วยเคยมีประวัติเป็น pulmonary embolism หรือ deep vein thrombosis มาก่อนจะถือเป็นข้อห้ามในการกินยาคุมกำเนิดอย่างเด็ดขาด. แต่สำหรับผู้ป่วยทั่วๆ ไปอุบัติการณ์การเกิด pulmonary embolism หรือ deep vein thrombosis จากยาคุมกำเนิดถือว่าต่ำมากสามารถใช้ได้อย่างปลอดภัย.
=ภาวะตั้งครรภ์ ส่วนใหญ่มักพบ pulmonary embolism ในช่วงระหว่างตั้งครรภ์ได้บ่อยกว่าช่วงหลังคลอด โดยเฉพาะอย่างยิ่งถ้าหากมารดามีอายุมาก และทำผ่าตัดคลอดโดยวิธี caesarean section จะทำให้เพิ่มความเสี่ยงต่อการเกิดภาวะนี้ มากขึ้นไปอีก.
=การรักษาด้วยฮอร์โมนในหญิงวัยหมดประจำเดือน จากการศึกษาขนาดใหญ่ของ The Women 's Health Initiative4 พบว่าอุบัติการณ์ของ pulmonary embolism มากขึ้นเป็น 2 เท่าในกลุ่มที่ได้รับฮอร์โมน และเพิ่มเป็น 3.5 เท่าในช่วงปีแรกที่ได้รับยา.
=โรคมะเร็ง ในบางครั้งสามารถพบ pulmonary embolism นำมาก่อนแล้วจึงวินิจฉัยมะเร็งได้ในภายหลัง และส่วนมากมักจะเป็นมะเร็งระยะที่แพร่กระจายแล้ว จึงควรตั้งข้อสงสัยทุกครั้งที่ตรวจพบ pulmonary embolism หรือ deep vein thrombosis ที่กลับเป็นซ้ำหลายๆ ครั้งและยังหาสาเหตุไม่พบว่าอาจมีโรคมะเร็งร่วมด้วยก็ได้.
3. ภาวะการแข็งตัวของเลือดผิดปกติ (thrombophilia) พบได้ทั้งชนิดที่ถ่ายทอดทางพันธุกรรมและที่เกิดขึ้นภายหลัง เช่น Factor V Leiden, hyperhomocysteinaemia, antiphospholipid antibody syndrome เป็นสาเหตุที่ทำให้ผู้ป่วยมาด้วย venous thromboembolism ได้บ่อย.
4. การเดินทางทางอากาศเป็นระยะเวลานาน โดยเฉพาะระยะทางมากกว่า 5,000 กม. ความเสี่ยงจะยิ่งมากขึ้นในผู้อายุมากกว่า 50 ปี, มีประวัติ thromboembolism มาก่อน, เป็นมะเร็ง เป็นต้น.
พยาธิสรีรวิทยา
ตาม Virchow 's triad การเกิดลิ่มเลือดในหลอดเลือดดำต้องประกอบด้วย venous stasis, endothelial damage, และ hypercoagulable states. ส่วนใหญ่ของผู้ป่วย pulmonary embolism มักมีต้นกำเนิดของลิ่มเลือดมาจากอุ้งเชิงกรานหรือหลอดเลือดดำที่ขา ซึ่งหลุดลอยไปสู่ pulmonary circulation ทำให้มี pulmonary vascular resistance สูงขึ้น, มีการแลกเปลี่ยนก๊าซบกพร่องจาก alveolar dead space ที่มากขึ้น และยังมีภาวะ hypoxemia จาก right-to-left shunt ร่วมด้วย เกิดการคั่งของคาร์บอนมอนอกไซด์ ร่างกายจะมีกลไกในการทำให้เกิด alveolar hyperventilation ตามมา.
นอกจากนี้ ผลจากการอุดตันของหลอดเลือดปอดยังทำให้มีการหลั่งสารเคมีที่มีฤทธิ์กระตุ้นให้หลอดเลือดเล็กๆ ในปอดตีบแคบลง ส่งผลให้ right ventricle ทำงานมากขึ้นจนอาจเกิด right ventricular failure ทำให้การสูบฉีดเลือดเสียไปจนอาจเป็นสาเหตุของการเสียชีวิตได้. อีกกลไกหนึ่งที่เป็นสาเหตุการเสียชีวิตที่สำคัญ ได้แก่ การเพิ่มความดันใน right ventricle ส่งผลต่อการทำงานของ left ventricle ทำให้ coronary perfusion pressure ลดลงทำให้เกิด right ventricular infarction และอาจเกิด cardiac arrest ตามลำดับ.
การวินิจฉัย
ดังได้กล่าวแล้วว่าอาการแสดงทางคลินิกของ pulmonary embolism มีได้หลากหลายขึ้นกับขนาดของลิ่มเลือดและบริเวณของหลอดเลือดปอดที่ถูกอุดตัน โดยอาจจะคล้ายคลึงกับภาวะหรือโรคอื่นๆ เช่น acute coronary syndrome, exacerbation of COPD เป็นต้น. และโดยเฉพาะอย่างยิ่งถ้าหากมีภาวะต่างๆ เหล่านั้นร่วมด้วยกับ pulmonary embolism การวินิจฉัยก็จะยิ่งทำได้ยากขึ้น. การวินิจฉัย ภาวะ pulmonary embolism ได้นั้นจำเป็นจะต้องมีเงื่อนงำบางประการที่ทำให้สงสัยว่าผู้ป่วยอาจจะมีโอกาสของการเกิดโรคในกลุ่ม venous thromboembolism ทั้งนี้มีผู้ทำการศึกษาถึงการประเมินความเป็นไปได้ในการวินิจฉัย pulmonary embolism จากการใช้ลักษณะต่างๆ ทางคลินิกโดยตัวอย่างของลักษณะที่ทำให้นึกถึงภาวะนี้มากขึ้น ได้แก่ อาการและอาการแสดงของ deep vein thrombosis, ไม่มีการวินิจฉัยอื่นๆ ที่จะเป็นไปได้มากกว่า pulmonary embolism, ชีพจรมากกว่า100 ครั้ง/นาที, ไม่ค่อยเคลื่อนไหวหรือได้รับการผ่าตัดในช่วง 4 สัปดาห์ที่ผ่านมา, เคยเป็น deep vein thrombosis หรือ pulmonary embolism มาก่อน, ไอเป็นเลือดและเป็นมะเร็งที่เพิ่งได้รักษาหรือภายในเวลาไม่เกิน 6 เดือน.5
อย่างไรก็ตาม การจะวินิจฉัยภาวะนี้ให้ถูกต้องและแม่นยำ คงต้องอาศัยการตรวจทางห้องปฏิบัติการอื่นๆ ร่วมด้วย (ภาพที่ 1).
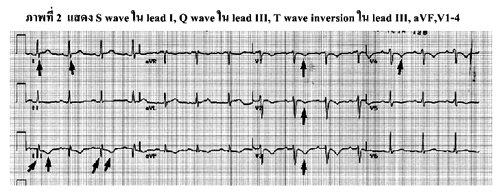
คลื่นไฟฟ้าหัวใจ (electrocardiogram) (ภาพที่ 2)
สามารถใช้แยกภาวะกล้ามเนื้อหัวใจขาดเลือดหรือภาวะเยื่อหุ้มหัวใจอักเสบได้. สำหรับภาวะ large pulmonary embolism นั้นจะพบลักษณะของ pulmonary hypertension และ right ventricular strain โดยอาจมี right bundle branch block, T-wave inversion ใน leads V1-4 , หรือ S1Q3T3 pattern.
ภาพรังสีทรวงอก (chest radiography)
มีประโยชน์ในการวินิจฉัยแยกโรคอื่นๆ เช่น ปอดอักเสบ, ลมรั่วในเยื่อหุ้มปอด, กระดูกซี่โครงหักและภาวะหัวใจล้มเหลว แต่ใน pulmonary embolism ก็อาจพบลักษณะผิดปกติบางอย่างเองได้ เช่นกรณี large pulmonary embolism อาจพบ cardiomegaly, enlarged pulmonary arteries หรือ oligaemia ของปอดด้านที่มีพยาธิสภาพ ส่วนในภาวะ small pulmonary embolism อาจพบลักษณะของ pulmonary infarction (" Hampton' s hump ") ซึ่งเป็น small wedge-shaped density อยู่ที่บริเวณส่วน periphery ของปอดได้.
การตรวจทางห้องปฏิบัติการ (laboratory studies)
= Arterial blood gas
ใช้ประเมินภาวะ hypoxemia และคำนวณค่า alveolar-arterial oxygen gradient ที่ค่ามักจะกว้างขึ้น ถือเป็นการตรวจเบื้องต้นทางห้องปฏิบัติการแต่ก็มีความไวและความจำเพาะเจาะจงไม่ดีนัก.
=D-dimer blood test
มักจะพบมีค่าสูงขึ้นในภาวะ acute pulmonary embolism แต่ทั้งนี้ไม่ได้มี ความจำเพาะเจาะจงต่อภาวะ pulmonary embolism เท่านั้น. D-dimer ยังสามารถสูงขึ้นได้ในหลายๆ ภาวะ เช่น กล้ามเนื้อหัวใจตาย, ปอดอักเสบ, ภาวะเลือดเป็นพิษ, มะเร็ง, การตั้งครรภ์หรือภาวะหลังการผ่าตัด เป็นต้น. ดังนั้น การตรวจในผู้ป่วยในอาจมีประโยชน์น้อยเนื่องจากผู้ป่วยมักมีภาวะผิดปกติบางประการที่ทำให้ค่า D-dimer สูงอยู่แล้ว แต่จะมีประโยชน์มากในการช่วยตรวจคัดกรองที่ห้องฉุกเฉินโดยกรณีที่ค่า D-dimer ปกติก็สามารถมั่นใจได้อย่างมากว่าไม่น่าจะมี pulmonary embolism(negative predictive value = ร้อยละ 99.6).7
=Cardiac biomarkers
พบว่า ระดับ troponin ที่สูงขึ้นมีความสัมพันธ์กับอัตราการเสียชีวิตโดยรวมและภาวะแทรกซ้อนขณะอยู่ในโรงพยาบาล เนื่องจากอาจเป็นตัวบ่งชี้ภาวะ right ventricular microinfarction.
Imaging studies
1. Ventilation/perfusion lung scan สำหรับการแปลผลนั้น ถ้าผลออกมาเป็น high-probability or normal lung scans นั้นก็ค่อนข้างเชื่อมั่นได้ว่ามีภาวะ pulmonary embolism หรือไม่มีภาวะนี้ตามลำดับ แต่ถ้าผลการตรวจเป็น intermediate probability จะยังไม่สามารถให้การวินิจฉัยภาวะนี้ได้.
2. CT chest ปัจจุบันถือว่าเป็นการตรวจที่มีประโยชน์เป็นอย่างมากสำหรับการวินิจฉัย pulmonary embolism. ข้อดีของวิธีนี้ก็คือ สามารถแสดงให้เห็นลิ่มเลือดที่อุดตันได้ ยกเว้นส่วนที่อยู่ภายในหลอดเลือดแขนงเล็กเกินไปและยังสามารถวินิจฉัยแยกโรคที่มีพยาธิสภาพในเนื้อปอดได้ด้วย. สำหรับ sensitivity ของการตรวจด้วย conventional CT chest เท่ากับร้อยละ 70 แต่ในปัจจุบันมี multi-row detector CT ซึ่งมี sensitivity เพิ่มขึ้นถึงมากกว่าร้อยละ 90.
3. Venous ultrasonography ถ้าตรวจพบว่ามี uncompressible vein เกิดขึ้นที่หลอดเลือดดำที่บริเวณขาหนีบ ก็สามารถให้การวินิจฉัยและรักษา deep vein thrombosis ได้เลย แต่ถ้าผลการศึกษาไม่พบความผิดปกติใดๆ ก็อาจจะยังไม่สามารถแยกภาวะ acute pulmonary embolismออกไปได้.
4. Pulmonary angiography เป็น gold standard สำหรับการวินิจฉัยภาวะ pulmonary embolism แต่เนื่องจากเป็นวิธีที่ invasive จึงควรพิจารณาทำเมื่อมีข้อบ่งชี้เป็นรายๆ ไป เช่น ในรายที่มีความสงสัยว่าเป็น pulmonary embolism แต่ยังไม่ได้การวินิจฉัยชัดเจนจากวิธีอื่น เป็นต้น.
5.Echocardiography ไม่สามารถนำไปใช้ในการวินิจฉัย pulmonary embolism ได้มากนัก.
การรักษา
1. Risk stratification
การประเมินความเสี่ยงของผู้ป่วย acute pulmonary embolism นั้น ทำให้สามารถเลือกการรักษาให้ผู้ป่วยได้อย่างเหมาะสม ถ้าเป็นกลุ่ม low risk การรักษาด้วย anticoagulant อย่างเดียวก็เพียงพอ. แต่สำหรับกลุ่ม high risk อาจต้องพิจารณาวิธีการรักษาด้วย thrombolysis หรือ embolectomy ความเสี่ยงของผู้ป่วยแต่ละรายได้จากการประเมินข้อมูลหลายๆ ด้าน เช่น การศึกษาของ Geneva prognostic index8 พบว่าลักษณะดังต่อไปนี้เป็นตัวบ่งชี้พยากรณ์โรคที่ไม่ดี ได้แก่ เป็นมะเร็งร่วมด้วย,มีภาวะหัวใจล้มเหลว, เคยเป็น deep vein thrombosis มาก่อน, มีความดันเลือดต่ำ,มีภาวะขาดออกซิเจน หรือตรวจพบ deep vein thrombosis จาก ultrasonography.
นอกจากนี้ก็ยังพบว่ามีลักษณะอื่นๆ อีกที่บ่งถึงพยากรณ์โรคที่ไม่ดีเช่น มีค่า troponin สูงขึ้น, echocardiography พบมี right ventricular dysfunction.
2.การให้ยา
2.1ยาป้องกันการแข็งตัวของเลือด
Heparin ยังคงเป็นยาหลักในการรักษาภาวะ acute pulmonary embolism ปริมาณที่ใช้ เริ่มด้วย 5,000-10,000 ยูนิต ตามด้วยการหยดทางหลอดเลือดดำในขนาด 18 ยูนิต/กก./ชั่วโมง หรือประมาณ 1,250 ยูนิต/ชั่วโมง ให้ระดับของ PTT อยู่ในเกณฑ์ที่ใช้รักษาคือ 60-80 วินาที. สำหรับปัจจุบันมีการนำเอา LMWH (low-molecular weight heparins) มาใช้ในการรักษาเนื่องจากสะดวกกว่าไม่ต้องปรับขนาดยา. ตัวอย่างเช่นยา enoxaparin ฉีดใต้ผิวหนังในขนาด 1 มก./กก.วันละ 2 ครั้งหรือ 1.5 มก./กก. วันละครั้ง ให้ผลต่อการรักษาไม่แตกต่างจาก unfractionated heparin เดิม.9 ภาวะแทรกซ้อนที่พบได้คือ ภาวะเลือดออก ส่วนน้อยที่อาจพบได้คือภาวะ heparin-induced thrombocytopenia with thrombosis มักพบส่วนใหญ่ภายหลังจากได้รับ heparin ภายในช่วง 4-14 วันแรก กรณีที่ให้ heparin เพื่อรอฤทธิ์ของยาป้องกันการแข็งตัวของเลือดชนิดกิน เช่น warfarin ต้องใช้เวลาประมาณ 5 วัน. ดังนั้น จึงควรให้ทั้ง 2 กลุ่มนี้ไปพร้อมๆ กันตั้งแต่ต้น และตรวจวัดระดับ INR ในเลือดให้อยู่ประมาณ 2-3 จึงถือว่าระดับของยาเพียงพอ. ขนาดยาส่วนใหญ่จะเริ่มด้วย warfarin ขนาด 5 มก. และจะต้องมีการติดตามปรับขนาดยาเป็นระยะๆ เพื่อป้องกันไม่ให้เกิดภาวะเลือดออกจากการได้ยาเกินขนาด ทั้งนี้ควรระวังเรื่องการบริหารยานี้ร่วมกับยาอื่นๆ เนื่องจากมี drug interaction ค่อนข้างมาก.
ระยะเวลาของการรักษาให้ดูจากสาเหตุตั้งต้นเป็นหลัก ถ้าหาก acute pulmonary embolism เป็นจากภาวะหลังผ่าตัด, การไม่เคลื่อนไหวนานๆ, หลังอุบัติเหตุพิจารณาให้ยาป้องกันการแข็งตัวของเลือดนานประมาณ 6 เดือน แต่กรณีที่ไม่ทราบสาเหตุอาจต้องให้นานกว่า 6 เดือน. นอกจากนี้ยังมียาขนานใหม่ที่นำมาใช้ได้ผลดีเช่นกัน ได้แก่ ximelagatran ซึ่งเป็นยาในกลุ่ม direct thrombin inhibitor สามารถลดอัตราการเกิดซ้ำ venous thromboembolism ได้ถึงร้อยละ 84.
2.2 ยาละลายลิ่มเลือด (thrombolysis), การผ่าตัด embolectomy
มีข้อบ่งชี้ในรายที่มีภาวะ acute massive pulmonary embolism ร่วมกับภาวะ cardiogenic shock แต่ยังเป็นข้อถกเถียงถึงการให้ thrombolysis ในผู้ป่วย ที่มี right ventricular dysfunction แต่มีความดันเลือดปกติ. อย่างไรก็ตาม พึง ควรระมัดระวังผลข้างเคียงจากการมีเลือดออกโดยเฉพาะในสมองไว้เสมอ.
สำหรับผู้ป่วยที่มีความเสี่ยงสูงที่จะเกิดภาวะเลือดออกได้ง่ายจากยา ป้องกันการแข็งตัวของเลือดหรือผู้ที่มีภาวะ recurrent pulmonary embolism แม้ในขณะที่ได้รับยาดังกล่าวอยู่อาจพิจารณาใส่ inferior vena caval filter เพื่อเป็นการป้องกันต่อไป.
3.การป้องกัน (prophylaxis)
ในต่างประเทศอาจพิจารณาการป้องกันในผู้ป่วยที่มีความเสี่ยงสูง แต่ในประเทศไทยไม่พบอุบัติการณ์สูงเช่นในต่างประเทศ จึงยังไม่มีข้อแนะนำดังกล่าว. ส่วนในผู้ป่วยที่เคยเป็น venous thromboembolism มาแล้วจะมีโอกาสเกิดซ้ำได้สูงภายในเวลา 10 ปีต่อมา. ดังนั้นหลังจากหยุดยาป้องกันการแข็งตัวของเลือดแล้วก็อาจติดตามอาการเพื่อเฝ้าระวังการเกิดซ้ำ หรือการตรวจวัดระดับของ D-dimer ก็อาจช่วยบอกถึงการเกิดซ้ำของโรคได้เช่นกัน โดยเฉพาะเมื่อระดับอยู่ในเกณฑ์ปกติจะมั่นใจได้อย่างมากว่าไม่มีการเกิดซ้ำในขณะนั้น.
เอกสารอ้างอิง
1. Carson JL, Kelley MA, Duff A, et al. The clinical course of pulmonary embolism. N Engl J Med 1992;326:1240-5.
2. Heit JA, Silverstein MD, Mohr DN, et al. Predictors of survival after deep vein thrombosis and pulmonary embolism : a population-based, cohort study. Arch Intern Med 1999;159:445-53.
3. Goldhaber SZ, Grodstein F, Stampfer MJ, et al. A prospective study of risk factors for pulmonary embolism in women. JAMA 1997;277:642-5.
4. Nelson HD, Humphrey HL, Nygren P, et al. Postmenopausal hormone replacement therapy : scientific review. JAMA 2002;288:872-81.
5. Wells PS, Anderson DR, Rodger M, et al. Derivation of a simple clinical model to categorize patients probability of pulmonary embolism : increasing the models utility with the SimpliRed D-dimer. Thromb Haemost 2000;83:416-20.
6. Goldhaber SZ. Pulmonary embolism. The Lancet 2004;363:1295-305.
7. Dunn KL, Wolf JP, Dorfman DM, et al. Normal D-dimer level in emergency department patients suspected of acute pulmonary embolism. J Am Coll Cardiol 2002;40:1475-8.
8. Wicki J, Perrier A, Perneger TV, et al. Predicting adverse outcome in patients with acute pulmonary embolism : a risk score. Thromb Haemost 2000;84:548-52.
9. Merli G, Spiro TE, Olsson CG, et al. Subcutaneous enoxaparin once or twice daily compared with intravenous unfractionated heparin for treatment of venous thromboembolic disease. Ann Intern Med 2001;134:191-202.
ดิลก ภิยโยทัย พ.บ., ผู้ช่วยศาสตราจารย์, สาขาอายุรศาสตร์, คณะแพทยศาสตร์, มหาวิทยาลัยธรรมศาสตร์ ศูนย์รังสิต
อิงอร อรุณากูร พ.บ., แพทย์ประจำบ้าน อายุรศาสตร์, ภาควิชาอายุรศาสตร์, คณะแพทยศาสตร์ศิริราชพยาบาล, มหาวิทยาลัยมหิดล
- อ่าน 35,106 ครั้ง
 พิมพ์หน้านี้
พิมพ์หน้านี้




