บทนำ
โรคเบาหวาน (diabetes mellitus) จัดเป็นปัญหาทางคลินิกที่สำคัญในกลุ่มโรคเรื้อรังซึ่งเกิดจากภาวะความไม่สมดุลของฮอร์โมนที่ทำหน้าที่ควบคุมระดับน้ำตาลกลูโคสในร่างกาย ทำให้ร่างกายไม่สามารถใช้น้ำตาลได้เต็มที่ น้ำตาลที่มีอยู่จึงเข้าไปสู่กระแสเลือดในระดับสูงกว่าปกติเป็นเวลานาน จึงเกิดอาการผิดปกติและภาวะแทรกซ้อนทั้งที่รุนแรง เฉียบพลัน และชนิดที่เรื้อรังตามมาในผู้ป่วย เช่น โรคหลอดเลือดหัวใจโรคความดันโลหิตสูง ภาวะแทรกซ้อนทางตา ระบบประสาท และไต เป็นต้น.
ปัจจุบันพบว่ามีจำนวนผู้ป่วยเบาหวานมากขึ้นและคาดว่าจะมีจำนวนเพิ่มขึ้นในทุกๆ ปี ข้อมูลทางสถิติจากองค์การอนามัยโลกที่ได้จากการสำรวจพบว่า ประชากรทั่วโลกเป็นเบาหวานประมาณ 140 ล้านคน ในจำนวนนี้เป็นชาวเอเชียประมาณ 82 ล้านคน ส่วนในประเทศไทยประเมินว่ามีผู้ป่วยเบาหวานประมาณ 2 ล้าน 5 แสนคน หรือประมาณร้อยละ 4 ของประชากรทั้งประเทศไทย.1,2
ภาวะที่ระดับน้ำตาลในเลือดสูงกว่าปกติของ ผู้ป่วยเบาหวานเกิดเนื่องจากสาเหตุที่สำคัญคือ ความผิดปกติของระดับฮอร์โมนอินซูลิน (insulin) ในร่างกาย กล่าวคือเกิดความบกพร่องในการผลิตอินซูลินจากตับอ่อน หรืออาจเกี่ยวข้องกับการลดการตอบสนองของอินซูลินต่อเนื้อเยื่อที่มีการนำน้ำตาลไปใช้ในร่างกาย (insulin resistance) ซึ่งภาวะดื้อ ต่ออินซูลินมักพบในคนอ้วนและผู้ที่มีระดับไขมันในเลือดสูงมากกว่าปกติ (hyperlipidemia).
การเกิดโรคเบาหวานชนิดที่ 2 ร่วมกับภาวะ ไขมันในเลือดสูงจัดเป็นภาวะที่พบได้บ่อย ซึ่งการรักษาผู้ป่วยที่มีภาวะดังกล่าวนิยมให้ยาควบคุมระดับน้ำตาล และยาควบคุมระดับไขมันในเลือดร่วมกัน ปัจจุบันจึง ได้มีการพัฒนายาที่สามารถควบคุมทั้งระดับน้ำตาลและระดับไขมันในเลือดโดยออกฤทธิ์ผ่าน peroxi-some proliferator-activated receptors (PPARs) ทั้งชนิด PPAR-a และ PPAR-g (PPAR-a/g dual agonist) ยาตัวแรกที่ได้มีการพัฒนาขึ้นคือ muraglitazar ซึ่งจัดอยู่ในกลุ่ม glitazars
.
Peroxisome proliferator-activated receptors (PPARs)
Peroxisome proliferator-activated recep-tors (PPARs) เป็นกลุ่มของ nuclear hormone receptor ซึ่งในตระกูล PPARs ประกอบด้วย 3 ชนิด ได้แก่ PPARa, PPARb/d และ PPARg โดยในแต่ละชนิด จะถูกควบคุมด้วยยีนที่แตกต่างกันทำให้ การทำหน้าที่ของพวกมันมีความหลากหลายในร่างกาย ขึ้นกับตำแหน่งที่มีการแสดงออกของยีนเหล่านี้ในเซลล์และเนื้อเยื่อ3,4 ดังแสดงในตารางที่ 1
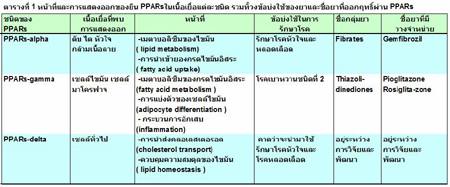
เช่น PPARa พบมากในบริเวณเนื้อเยื่อไขมัน และพบได้น้อยในเซลล์กล้ามเนื้อ, endothelial cells, vascular smooth muscle cell, macrophage และ colonic epithelium ซึ่ง PPARa มีหน้าที่เกี่ยวข้องกับการควบคุมการทำงานของ fatty acid ในขั้นตอน cellular uptake, activation และควบคุมการทำงานของ fatty acid transport protein สำหรับ PPARb/d จะมีอยู่ในเนื้อเยื่อทั่วไป ส่วนใหญ่ทำหน้าที่สำคัญในกระบวนการ lipid และ lipoprotein metabolism ร่วมกับ PPARa ส่วน PPARg พบมากในเซลล์ไขมัน (adipose tissue) และ เซลล์ตับ ซึ่งมีหน้าที่สำคัญเกี่ยวข้องกับการแบ่งตัวของเซลล์ไขมัน (adipocyte differentiation) ควบคุมกระบวนการเมตาโบลิซึมของไขมันและกลูโคส (lipid and glucose homeostasis) และควบคุมการหลั่งอินซูลินในร่างกาย.
PPARs จัดเป็น ligand dependent transcription factor ที่ควบคุมการแสดงออกของยีนเป้าหมายหลายชนิดโดยที่ตัวมันเองสามารถจับกับลำดับเบสจำเพาะที่เรียกว่า PPRE (PPAR responsive element) ในบริเวณ enhancer site ของยีนเป้าหมายเหล่านั้น โดย PPRE เป็นลักษณะของลำดับเบสซ้ำ (direct repeated sequence) ซึ่งประกอบด้วย 6 นิวคลีโอไทด์ (hexanucleotides) คือ AGGNCA เมื่อ N แทนลำดับเบสใดๆ ตัวอย่างของยีนเป้าหมาย ที่มี PPRE เป็นส่วนประกอบ เช่น acyl-CoA oxidase, adipocyte fatty acid-binding protein, lipoprotein lipase และ GLUT เป็นต้น.
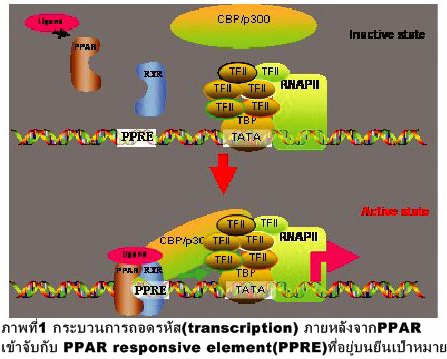
โดยทั่วไป PPAR จะจับบน PPRE บนยีนเป้าหมาย โดยมีโปรตีน retinoid X receptor (RXR) จับร่วมกับ PPAR เป็นลักษณะ heterodimer-DNA sequence complex อยู่ภายในนิวเคลียส ดังภาพที่ 1 เมื่อ PPAR ถูกกระตุ้นโดย PPAR-ligand จะมีผลให้รูปร่างของ PPAR เปลี่ยนแปลงเป็นรูปแบบที่มีความเสถียรมากขึ้น จึงเกิดเป็นตำแหน่งที่เหมาะสมสำหรับให้โปรตีนจำพวก coactivators เช่น CEB/p300 และ steroid receptor coactivator (SRC)-1 มาจับได้ง่ายขึ้น ดังนั้นจึงเกิดการเหนี่ยวนำให้เกิดกระบวนการถอดรหัส (transcription) ของยีนเป้าหมายได้ในที่สุด.
ในปัจจุบันมียาที่ออกฤทธิ์ผ่านการทำงานของ PPAR-a และ PPAR-g แต่ยังไม่มียาที่ออกฤทธิ์ผ่านการทำงานของ PPAR-d. ยาที่ออกฤทธิ์ผ่านการทำงานของ PPAR-a คือยาในกลุ่ม fibrates ได้แก่ bezafibrate และ gemfibrozil โดยยากลุ่มนี้จะมีผลทำให้ระดับ triglycerides และ LDL-cholesterol ลดลง และมีผลเพิ่มระดับ HDL-cholesterol จึงเป็น ผลดีในการลดระดับไขมันในเลือด. ส่วนยาที่ออกฤทธิ์ ผ่านการทำงานของ PPAR-g คือยาในกลุ่ม thiazolidinediones (TZDs) ได้แก่ pioglitazone และ rosiglitazone โดยยากลุ่มนี้มีผลทำให้ลดการสร้างน้ำตาลกลูโคสในตับและมีผลให้เกิดการเปลี่ยนแปลงของเซลล์ไขมันโดยทำให้มีขนาดเล็กลง (adipocyte differentiation) จึงเพิ่มระดับ adiponectin และลดระดับ free fatty acid และ resistin ในกระแสเลือดส่งผลเพิ่มความไวของอินซูลินและเพิ่มการนำน้ำตาลเข้าสู่เซลล์ตับและกล้ามเนื้อลาย จึงทำให้ระดับน้ำตาลในเลือดลดลงในที่สุด.5,6
การออกฤทธิ์กระตุ้นการทำงานของ PPAR-a และ PPAR-g ทำให้ระดับไขมันและน้ำตาลในเลือดลดลง ตามลำดับ ดังนั้นจึงมีการพัฒนายาที่ออกฤทธิ์ผ่านการทำงานของทั้ง PPAR-a และ PPAR-g (PPAR-a/g dual agonist) เพื่อนำมาใช้ในการรักษาโรคเบาหวานที่มีภาวะไขมันในเลือดสูงร่วมด้วย. ยาตัวแรกที่มีการพัฒนาขึ้นมาคือ muraglitazar จัดอยู่ในกลุ่ม glitazars ซึ่งผ่านการพิจารณาและรับรองจากคณะกรรมการอาหารและยาของสหรัฐอเมริกา (US Food and Drug Administration) เมื่อเดือนตุลาคม 2548 สำหรับใช้รักษาโรคเบาหวานชนิดที่ 2 ซึ่งมีการศึกษาทางคลินิกทั้งในรูปแบบที่มีการรักษาแบบเดี่ยว (monotherapy) และการรักษาร่วมกับยาลดระดับน้ำตาลอื่นๆ (combination therapy) เช่น sulfonylureas หรือ metformin.7,8
ลักษณะโครงสร้างทางเคมี
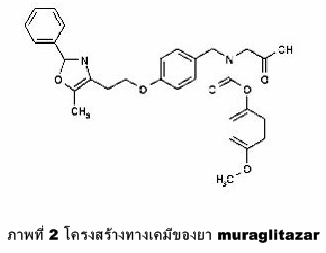
Muraglitazar จัดเป็นยาในกลุ่ม non-thiazolidinedione9 ลักษณะโครงสร้างเป็น oxybenzyl- glycine ดังแสดงในภาพที่ 2. ยาชนิดนี้ถูกพัฒนาขึ้น มาให้มีความสามารถในการจับได้ทั้ง PPAR-a และ PPAR-g อย่างจำเพาะเจาะจง ที่เรียกว่า PPAR-a/g dual agonist โดยมีความสามารถในการจับกับ PPAR-g (IC50= 0.14 mM) ได้ดีกว่า PPAR-a (IC50 =0.42 mM) แต่ไม่สามารถจับกับ nuclear hormone receptor ตัวอื่นๆ ได้ เช่น PPAR-d, retinoic acid receptor-alpha (RXRa), estrogen receptor alpha and beta (ERa/b).
ฤทธิ์ทางเภสัชวิทยา
Muraglitazar จัดอยู่ในกลุ่ม glitazars ซึ่งมีฤทธิ์ควบคุมระดับไขมันในเลือดเพื่อลดระดับ triglyceride และเพิ่มระดับ HDL-cholesterol ได้คล้ายกับยาในกลุ่ม fibrates รวมทั้งมีฤทธิ์ควบคุมระดับน้ำตาลในเลือดและเพิ่มความไวต่ออินซูลินได้คล้ายกับยาในกลุ่ม TZDs ซึ่งฤทธิ์ในการลดระดับน้ำตาลและไขมันในเลือดได้ในคราวเดียวกันนี้จึงนำมาใช้ประโยชน์ในการรักษาโรคเบาหวานชนิดที่ 2 ที่มีภาวะไขมันในเลือดสูงร่วมกัน7,8
เภสัชจลนศาสตร์
เภสัชจลนศาสตร์ของยา muraglitazar ได้มี การศึกษาทั้งในอาสาสมัครสุขภาพดีและกลุ่มผู้ป่วยเบาหวานชนิดที่ 2 พบว่ายาถูกดูดซึมได้อย่างรวดเร็วและตรวจวัดระดับยาในเลือดได้ภายใน 30 นาที โดย มีช่วงเวลาการดูดซึมยาได้มากที่สุด (Tmax) อยู่ระหว่างชั่วโมงที่ 1 และชั่วโมงที่ 6 ค่าครึ่งชีวิต (half-life) ของยาอยู่ระหว่าง 19-27 ชั่วโมง ดังนั้นจึงแนะนำให้ผู้ป่วยรับประทานยาวันละ 1 ครั้ง.
การเปลี่ยนแปลงยา muraglitazar เกิดขึ้นที่ตับโดยผ่านทั้งในระยะที่1 (phase 1)และระยะที่ 2 (phase 2)10-12 ซึ่งกระบวนการหลักที่ใช้ในการเปลี่ยน แปลงยา คือ glucoronidation, hydroxylation และ
O-demethylation ยาส่วนใหญ่ถูกขับออกทางน้ำดี มีเพียงส่วนน้อยที่ถูกขับออกทางไต (น้อยกว่าร้อยละ 4) ดังนั้นจึงไม่จำเป็นต้องปรับขนาดยาในผู้ป่วยที่มีภาวะการทำงานของไตบกพร่อง.
Muraglitazar เป็นสารตั้งต้นของเอนไซม์ CYP450 หลายชนิด ได้แก่ CYP3A4, CYP2C19, CYP2C9, CYP2C8 และ CYP2D6 จากการศึกษาทางคลินิกพบว่าการให้ยา muraglitazar ร่วมกับ ketoconazole ซึ่งเป็น CYP3A4 inhibitor หรือการให้ยา muraglitazar ร่วมกับ gemfibrozil ซึ่งเป็น CYP2C8 inhibitor มีผลเพิ่มความเข้มข้นของยาสูงสุดในเลือด (Cmax) ร้อยละ 23 ถึง 27 ดังนั้นจึงจำเป็นต้องระมัดระวังการใช้ยาร่วมกันสำหรับยาทั้งสองชนิดนี้. ส่วนการศึกษาทางด้านเภสัชจลนศาสตร์กับเอนไซม์ตัวอื่น เช่น CYP2C9 (S-warfarin), CYP2C19 (R-warfarin) และ CYP3A4 (atrovastatin หรือ sim-vastatin) หรือยาลดระดับน้ำตาลในเลือด และยาลดระดับไขมันในเลือดอื่นๆ เช่น metformin, pravastatin และ fenofibrate พบว่าไม่ทำให้เกิดการเปลี่ยน แปลงของระดับยา muraglitazar นอกจากนี้การให้ ยา muraglitazar กับอาหารที่มีไขมันสูงหรือยาที่เพิ่ม pH ในกระเพาะอาหารเช่น famodine พบว่าไม่มีผลต่อค่า AUC.
ข้อบ่งใช้และขนาดยา
Muraglitazar มีข้อบ่งใช้ในผู้ป่วยโรคเบาหวานชนิดที่ 28 โดยอาจใช้เป็นการรักษาแบบเดี่ยว (monotherapy) หรือใช้ร่วมกับยาลดระดับน้ำตาลอื่นๆ (combination therapy) เช่น sulfonylureas หรือ met formin. การพิจารณาให้ยา muraglitazar ร่วมกับยาลดระดับน้ำตาลอื่นๆ นั้น นิยมใช้ในกรณีที่ผู้ป่วยไม่สามารถควบคุมระดับน้ำตาลได้อย่างเหมาะสมด้วยยาลดระดับน้ำตาลในกลุ่มอื่นๆ จากการศึกษาทางคลินิกพบว่าผู้ป่วยที่ได้รับยาแบบ combination therapy สามารถควบคุมระดับน้ำตาลและระดับไขมันในเลือดได้ดีกว่าการได้รับยาลดระดับน้ำตาลในกลุ่ม sulfonylureas หรือยา metformin แบบเดี่ยว13 ขนาดของยา muraglitazar ที่มีการผลิตและจำหน่ายคือ ขนาด 2.5 มก. และ 5 มก. โดยขนาดเริ่มต้นที่แนะนำให้ผู้ป่วยคือ 2.5 มก. และอาจปรับขนาดยาเป็น 5 มก. สำหรับผู้ป่วยที่มีภาวะน้ำตาลในเลือดสูงหรือมีระดับไขมันผิดปกติ ซึ่งยา muraglitazar ทั้งสองขนาดนี้แนะนำให้รับประทานวันละ 1 ครั้ง.
อาการไม่พึงประสงค์จากการใช้ยา
จากการศึกษาทางคลินิกพบว่าการใช้ยา muraglitazar ขนาด 2.5 และ 5 มก. มีความปลอดภัยในระดับหนึ่งสำหรับใช้ในการรักษาโรคเบาหวานชนิดที่ 2. อย่างไรก็ตาม มีรายงานเหตุการณ์ไม่พึงประสงค์จากการใช้ยาที่เกิดขึ้น ได้แก่ ภาวะหัวใจล้มเหลวน้ำหนักตัวเพิ่มและการบวมน้ำ แต่ยังไม่พบรายงานเกี่ยวกับการเกิดพิษต่อตับ กล้ามเนื้อ และไต.14,15
ภาวะหัวใจล้มเหลวเป็นเหตุการณ์ไม่พึงประสงค์ที่สำคัญมากที่สุดสำหรับการใช้ยาชนิดนี้ แต่อัตราการเกิดภาวะหัวใจล้มเหลวนั้นพบได้ไม่บ่อยมากนัก โดยพบได้ร้อยละ 0.19 และ 0.34 ในอาสาสมัครที่ได้รับยา muraglitazar ขนาด 2.5 มก. และขนาด 5 มก. ตามลำดับ ซึ่งผู้ป่วยที่มีความผิดปกติเกี่ยวกับหัวใจและหลอดเลือดควรระมัดระวังในการใช้ยาชนิดนี้ การเพิ่มขึ้นของน้ำหนักตัวจากการใช้ยาก็เป็นอีกปัญหาหนึ่งสำหรับผู้ป่วย ซึ่งสาเหตุของการเกิดนั้นมาจากการออกฤทธิ์กระตุ้นการทำงานของ PPAR-g ในเซลล์ไขมัน โดยพบว่าการใช้ยา muraglitazar ขนาด 2.5 และ 5 มก. ทำให้น้ำหนักตัวเพิ่มขึ้นเฉลี่ย 1 กิโลกรัมและ 2.2 กิโลกรัม ตามลำดับ ส่วนภาวะบวมน้ำที่เกิดจากการใช้ยานั้นแปรผันโดยตรงกับขนาดของยาที่ได้รับ.16
ข้อควรระวังและข้อห้ามใช้14,15
1. ไม่แนะนำให้ใช้ในผู้ป่วยที่มีระดับน้ำตาลในเลือดไม่สูงมากนัก.
2. ไม่แนะนำให้ใช้ในผู้ป่วยที่ไม่สามารถทนต่อภาวะน้ำเกิน (fluid overload) เช่น ผู้ป่วยหัวใจล้มเหลวระดับ 2 (New York Heart Association (NYHA) class II).
3. ไม่แนะนำให้ใช้ในผู้ป่วยเบาหวานชนิดที่ 2 ที่มีอายุต่ำกว่า 18 ปี เนื่องจากขณะยังไม่มีข้อมูลการศึกษาในประชากรกลุ่มนี้.
4. ไม่ควรใช้ยานี้ร่วมกับยากลุ่ม thiazolidine-diones และ fibrates.
5. ห้ามใช้ในผู้ป่วยโรคหัวใจล้มเหลวระดับ 3 และ 4 (NYHA class III and IV).
พิษวิทยา
การศึกษาความเป็นพิษของยา muraglitazar ไม่พบการเกิดพิษอย่างเฉียบพลัน (acute toxicity) และความเป็นพิษต่อตับ ไต หัวใจและกล้ามเนื้อ รวมทั้งไม่พบการเกิดพิษก่อวิรูป (teratogenesis) ของตัวอ่อน. สำหรับการศึกษาการเกิดมะเร็ง (carcinogenesis) ในสัตว์ทดลองพบว่าได้ผลการทดลองที่แตกต่างกันทั้งนี้ขึ้นกับชนิดของสัตว์ทดลองและขนาดของยาที่ได้รับโดยมีรายงานการเกิดก้อนเนื้องอกในกระเพาะปัสสาวะ (urinary bladder tumors) ในหนูทดลองเพศผู้ แต่ไม่พบการเกิดเนื้องอกชนิดนี้ในลิงที่ได้รับยาที่มีขนาดมากกว่า 59 เท่าของขนาดที่ได้รับในมนุษย์. นอกจากนี้ ยังพบรายงานการเกิดเนื้องอกในถุงน้ำดี (gallbladder adenomas) ในหนูเพศผู้ซึ่งได้รับยาที่ มีขนาดมากกว่า 48 เท่าของขนาดที่ได้รับในมนุษย์.14-16 การศึกษาดังกล่าวข้างต้นแสดงให้เห็นว่าการเกิดมะเร็งจากการใช้ยา muraglitazar สามารถพบได้ในขนาด ยาที่สูงมาก ซึ่งข้อมูลความเป็นพิษเหล่านี้ยังไม่พบ การเกิดมะเร็งในมนุษย์ เนื่องจากขนาดของยาที่ให้ ในมนุษย์เป็นขนาดที่น้อยกว่าขนาดยาที่สัตว์ทดลองได้รับ.
บทสรุป
Muraglitazar จัดเป็นยาตัวแรกในกลุ่ม glitazars ซึ่งมีฤทธิ์ในการกระตุ้นการทำงานของทั้ง PPAR-a และ PPAR-g (PPAR-a/g dual agonist) โดยการพัฒนายานี้ได้นำเอาข้อบ่งใช้ที่เด่นชัดของยาทั้งสองชนิดมารวมกัน ได้แก่ ยาที่ออกฤทธิ์กระตุ้นการทำงานของ PPAR-a สำหรับการรักษาภาวะไขมันในเลือดสูง และยาที่ออกฤทธิ์กระตุ้นการทำงานของ PPAR-g สำหรับควบคุมระดับน้ำตาลในเลือดสูงในโรคเบาหวาน ชนิดที่ 2 ดังนั้นยา muraglitazar จึงมีข้อบ่งใช้ในผู้ป่วยโรคเบาหวานชนิดที่ 2 ที่มีระดับไขมันสูง โดยอาจใช้เป็นการรักษาแบบเดี่ยว (monotherapy) หรือใช้ร่วมกับยารักษาเบาหวานชนิดอื่น (combination therapy) เช่น sulfonylureas หรือ metformin ขนาดของยาที่แนะนำให้เริ่มใช้คือ 2.5 มก. สำหรับผู้ป่วยที่มีภาวะน้ำตาลในเลือดสูงหรือมีระดับไขมันผิดปกติ ควรใช้ยาขนาด 5 มก. โดยรับประทานวันละ 1 ครั้ง. อาการไม่พึงประสงค์จากการใช้ยาที่พบได้แก่ ภาวะหัวใจล้มเหลว น้ำหนักตัวเพิ่มและการบวมน้ำ ซึ่งผู้ป่วยที่มีความผิดปกติเกี่ยวกับโรคหัวใจและหลอดเลือดควรหลีกเลี่ยงการได้รับยาชนิด นี้ จากการศึกษาทางคลินิกไม่พบความเป็นพิษต่อตับ กล้ามเนื้อและไต. อย่างไรก็ตาม ความเป็นพิษและเหตุการณ์ไม่พึงประสงค์อื่นๆที่อาจเกิดขึ้นจาก การใช้ยายังคงต้องการข้อมูลเพิ่มเติมเพื่อยืนยันความปลอดภัยจากการใช้ยานี้ในอนาคต.
เอกสารอ้างอิง
1. Zimmet P. The burden of type 2 diabetes : are we doing enough? Diabetes Metab 2003;29(4 Pt 2):6S9-18.
2. World Health Organization. Diabetes Programme. [cited August 10, 2006]; Available from: http://www.who.int/diabetes/en/<
3. Cresci S. The PPAR genes, cardiovascular disease and the emergence of PPAR pharmacogenetics. Expert Opin Pharmacother 2005 Dec;6(15):2577-91.
4. Kersten S, Desvergne B, Wahli W. Roles of PPARs in health and disease. Nature 2000 May 25;405(6785):421-4.
5. Staels B, Fruchart JC. Therapeutic roles of peroxisome proliferator-activated receptor agonists. Diabetes 2005 Aug;54(8):2460-70.
6. Balint BL, Nagy L. Selective modulators of PPAR activity as new therapeutic tools in metabolic diseases. Endocr Metab Immune Disord Drug Targets 2006 Mar;6(1):33-43.
7. Barlocco D. Muraglitazar (Bristol-Myers Squibb/Merck). Curr Opin Investig Drugs 2005 Apr;6(4):427-34.
8. Cox SL. Muraglitazar : an agent for the treatment of type 2 diabetes and associated dyslipidemia. Drugs Today (Barc) 2005 Sep;41(9):579-87.
9. Devasthale PV, Chen S, Jeon Y, Qu F, Shao C, Wang W, et al. Design and synthesis of N-[(4-methoxypheno-xy)carbonyl]-N-[[4-[2-(5-methyl-2-phenyl-4-oxazolyl)-ethoxy] phenyl] methyl] glycine [Muraglitazar/BMS-298585], a novel peroxisome proliferator-activated receptor alpha/gamma dual agonist with efficacious glucose and lipid-lowering activities. J Med Chem 2005 Mar 24;48(6):2248-50.
10. Li W, Zhang D, Wang L, Zhang H, Cheng PT, Zhang D, et al. Biotransformation of carbon-14-labeled muraglitazar in male mice : interspecies difference in metabolic pathways leading to unique metabolites. Drug Metab Dispos 2006 May;34(5):807-20.
11. Wang L, Zhang D, Swaminathan A, Xue Y, Cheng PT, Wu S, et al. Glucuronidation as a major metabolic clearance pathway of 14c-labeled muraglitazar in humans : metabolic profiles in subjects with or without bile collection. Drug Metab Dispos 2006 Mar;34(3):427-39.
12. Zhang D, Zhang H, Aranibar N, Hanson R, Huang Y, Cheng PT, et al. Structural elucidation of human oxidative metabolites of muraglitazar : use of microbial bioreactors in the biosynthesis of metabolite standards. Drug Metab Dispos 2006 Feb;34(2):267-80.
13. Kendall DM, Rubin CJ, Mohideen P, Ledeine JM, Belder R, Gross J, et al. Improvement of glycemic control, triglycerides, and HDL cholesterol levels with muraglitazar, a dual (alpha/gamma) peroxisome proliferator-activated receptor activator, in patients with type 2 diabetes inadequately controlled with metformin monotherapy : A double-blind, randomized, pioglitazone-comparative study. Diabetes Care 2006 May;29(5):1016-23.
14. Najman DM. Adverse events related to muraglitazar use in diabetes. JAMA. 2006 May 3;295(17):1997; author reply 8.
15. Parra D, Beckey C, Thomas T. Adverse events related to muraglitazar use in diabetes. JAMA 2006 May 3;295(17):1997-8; author reply 8.
16. US FDA. Advisory Committe briefing document: Pargluva (muraglitazar, BMS-298585). [cited August 12, 2006]; Available from: http:www.fda.gov/ohrms/dockets/ac/ 05/briefing/2005-4169B2_01_01-BMS-Pargluva.pdf
อัจฉรา ศรีสดใส ภ.บ., ปร.ด., อาจารย์ คณะเภสัชศาสตร์ มหาวิทยาลัยขอนแก่น
ปฬาภรณ์ อันพาพรม, นักศึกษา, คณะเภสัชศาสตร์ มหาวิทยาลัยขอนแก่น
- อ่าน 12,590 ครั้ง
 พิมพ์หน้านี้
พิมพ์หน้านี้




