Acute respiratory distress syndrome (ARDS) เป็นภาวะหายใจล้มเหลวเฉียบพลันที่เกิดจากการที่เนื้อปอดมีพยาธิสภาพเกิดขึ้นอย่างรุนแรง กระจายอย่างรวดเร็วไปที่เนื้อปอดทั้ง 2 ข้าง เป็นผลให้มีภาวะพร่องออกซิเจนอย่างมาก หากไม่ได้รับการรักษาอย่างถูกต้องทันท่วงทีผู้ป่วยมีโอกาสเสียชีวิตได้มาก. 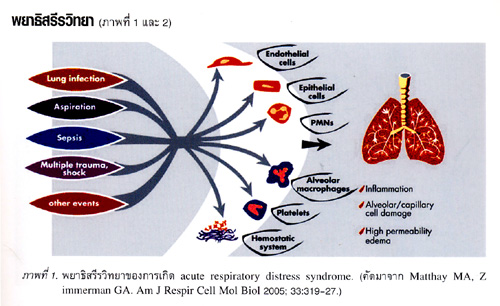
หลักเกณฑ์การวินิจฉัย ARDS1 ได้แก่
1. การเกิดภาวะหายใจล้มเหลวแบบเฉียบพลัน.
2. ภาพถ่ายรังสีทรวงอกพบว่ามี infiltrate จนทำให้เนื้อปอดดูขาวทั้ง 2 ข้าง.
3. ไม่มีความผิดปกติของหัวใจ โดยไม่พบว่ามี left atrial hypertension หรือวัด pulmonary artery wedge pressure ได้ น้อยกว่าหรือเท่ากับ 18 มม.ปรอท.
4. มีภาวะพร่องออกซิเจนอย่างรุนแรง โดยคำนวณอัตราส่วนของค่า PaO2/FiO2 ได้น้อยกว่าหรือเท่ากับ 200 มม.ปรอท.
สาเหตุ
อาจเป็นได้ทั้งจากความผิดปกติที่ปอดโดยตรง ที่พบบ่อย เช่น ปอดอักเสบจากการติดเชื้อ จมน้ำ สำลัก และความผิดปกติที่ระบบอื่นแต่ส่งผลกระทบมาที่ปอด เช่น sepsis, massive transfusion เป็นต้น.
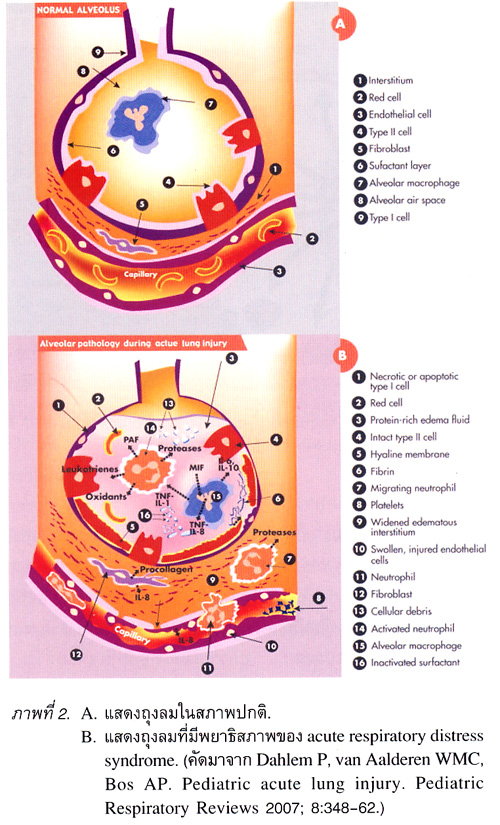
พยาธิสรีรวิทยา (ภาพที่ 1 และ 2)
พยาธิสภาพที่เนื้อปอดเป็นผลมาจากการที่ร่างกายได้รับการกระตุ้นจากสาเหตุต่างๆ ดังกล่าวข้างต้นทำให้มีการหลั่งสาร mediator หรือ cytokine ต่างๆ2 เช่น tumor necrosis factor, interleukin (IL)-1, IL-6, IL-8 เป็นผลให้มีการทำลายเนื้อเยื่อถุงลม มีการขยายตัวของหลอดเลือดฝอยรอบถุงลม มีเม็ดเลือดขาว เช่น neutrophil เคลื่อนที่เข้ามาใน ถุงลม ทำให้เกิดปฏิกิริยาของการอักเสบภายในถุงลมและรอบๆ ถุงลมอย่างต่อเนื่อง มีของเหลวโปรตีนสูง รั่วออกจากหลอดเลือดเข้ามาสะสมในถุงลมและ interstitium ทำให้เห็นคล้ายเป็น hyaline membrane ในถุงลม. กระบวนการอักเสบที่เกิดขึ้นดังกล่าวทำให้มีการเปลี่ยนแปลงของ surfactant ทั้งด้านปริมาณและคุณภาพ ทำให้ถุงลมแฟบ ความยืดหยุ่นของปอดลดลง เนื้อปอดแข็ง การแลกเปลี่ยนก๊าซออกซิเจนบกพร่องอย่างมาก เนื่องจากลมหายใจเข้าไม่สามารถเข้าไปถึงถุงลมได้ เกิดเป็น intrapulmonary shunt ในทางปฏิบัติจะเห็นว่าถึงแม้จะให้ออกซิเจนความ เข้มข้นสูงก็ไม่สามารถแก้ไขภาวะพร่องออกซิเจนได้.
อาการและอาการแสดง
ผู้ป่วยที่เป็น ARDS จะมีอาการของภาวะหายใจ ล้มเหลวเฉียบพลัน คือ หายใจเร็ว แรง หน้าอกบุ๋ม เขียว ความรู้สติลดลง irritable ฟังเสียงปอดได้ยินเสียง crepitation, bronchial breath sound ผู้ป่วยทุกรายเมื่อให้ออกซิเจนไม่ดีขึ้น มักจบลงด้วยการใส่ท่อหลอดลมคอ แล้วต่อกับเครื่องช่วยหายใจ.
การตรวจก๊าซในเลือดแดง
พบว่ามี PaO2 และ SaO2 ต่ำ ให้ FiO2 สูงก็ไม่สามารถเพิ่ม PaO2 และ SaO2 ได้ คำนวณสัดส่วนของ PaO2 / FiO2 ได้ น้อยกว่าหรือเท่ากับ 200 มม.ปรอท แต่ด้านการแลกเปลี่ยนก๊าซคาร์บอนไดออกไซด์มักจะไม่มีปัญหาเนื่องจาก CO2 แทรกซึมผ่านผนังถุงลมและหลอด เลือดฝอยได้ดีกว่า O2 ถึง 20 เท่า ส่วนใหญ่ในระยะแรกมักพบว่าก๊าซในเลือดแดงมีลักษณะเป็น respiratory alkalosis มี PaCO2 น้อยกว่าหรือเท่ากับ ปกติ.
ภาพถ่ายรังสีปอด
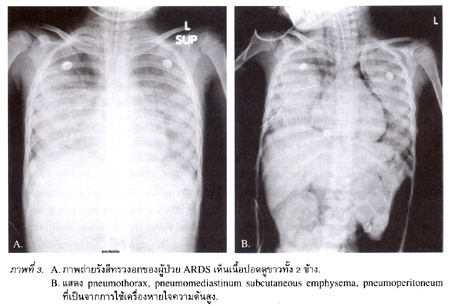
มักจะพบว่ามีเนื้อปอดขาวทั้ง 2 ข้าง (diffuse, fluffy alveolar infiltrate) และเห็น air bronchogram (ภาพที่ 3A) ถ้าส่งตรวจ CT scan ก็จะพบว่า มีฝ้าขาวเป็นปื้นๆ แบบ heterogeneous โดยปื้นที่เห็นจะหนาแน่นมากในส่วนที่เป็น dependent lung ทางด้าน posterior ของปอด.
การรักษา
นอกจากการรักษาแบบจำเพาะเจาะจงต่อสาเหตุที่ทำให้เกิด ARDS แล้ว การรักษาแบบประคับประคอง (supportive care) ให้พ้นวิกฤต เป็นหัวใจหลักที่จะช่วยรักษาชีวิตผู้ป่วยไว้ได้.
การรักษาแบบประคับประคองประกอบด้วย
1. การใช้เครื่องช่วยหายใจ.
2. ยา.
3. การดูแลรักษาด้านโภชนาการ สารน้ำ และเกลือแร่.
4. การรักษาและป้องกันปอดอักเสบแทรกซ้อนจากการใช้เครื่องช่วยหายใจ.
1. การใช้เครื่องช่วยหายใจ
การใช้เครื่องช่วยหายใจอย่างเหมาะสมจะ ช่วยลดภาระการหายใจ (work of breathing) ทำให้ ผู้ป่วยไม่ต้องออกแรงหายใจจนเหนื่อย ช่วยให้สามารถ เพิ่มความเข้มข้นของออกซิเจน (FiO2) ได้เต็มที่จนถึง 100% ช่วยถ่างถุงลมที่แฟบอยู่ให้เปิดออกดันลมหายใจให้เข้าไปถึงถุงลมได้มากขึ้น สามารถแลกเปลี่ยนก๊าซได้ดีขึ้น ลดการเกิด intrapulmonary shunt นอกจากนี้ยังช่วยลด venous return ทำให้ของเหลวรั่วซึมออกนอกหลอดเลือดฝอยรอบๆ ถุงลมลดลง.
ในทางตรงกันข้ามถ้าใช้เครื่องช่วยหายใจไม่เหมาะสมหรือมากเกินไป ก็จะทำให้เกิดภาวะแทรกซ้อน จนทำให้ผู้ป่วยถึงแก่ชีวิตได้.
อันตรายที่เกิดจากการใช้เครื่องช่วยหายใจ มักเป็นจากการใช้ความดันสูงมากเกิน (barotrauma) หรือ tidal volume ที่สูงเกิน (volutrauma) จนไปทำลายเนื้อเยื่อของถุงลม หรือทำให้ถุงลมถูกถ่างขยายจนมีขนาดใหญ่เกินไป (overdistention) รวมไปถึงการดันลมเข้าและออกจากถุงลมเป็นช่วงๆ ทำให้เกิดการกระชากเปิดปิดถุงลมที่แฟบอยู่ซ้ำแล้วซ้ำเล่า (atelectrauma). ถ้าถ่ายภาพรังสีทรวงอกก็จะเห็น pulmonary interstitial emphysema, pneumothorax, pneumomediastinum, subcutaneous emphysema, pneumoperitoneum, retroperitoneal air (ภาพที่ 3B) และ pneumopericardium.
การตั้งเครื่องช่วยหายใจในผู้ป่วย ARDS จะต้องทำอย่างสุขุม เพื่อหลีกเลี่ยงภาวะแทรกซ้อนข้างต้นให้มากที่สุด เรียกว่าเป็นวิธีการป้องกันอันตรายต่อเนื้อปอด (lung protective strategy).3
หลักใหญ่ในการตั้งเครื่องช่วยหายใจในผู้ป่วย ARDS4 ประกอบด้วย
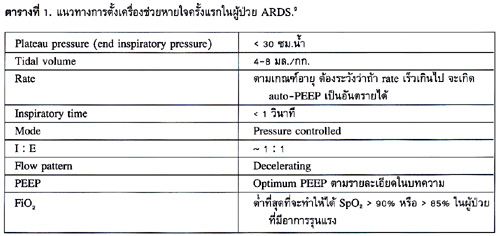
1. Plateau pressure หรือ alveolar pressure ควรน้อยกว่า 30 ซม.น้ำ.5
2. Tidal volume ควรตั้งประมาณ 6 มล./กก. ของ ideal body weight หรือระหว่าง 4-8 มล./กก.
3. ตั้ง positive end expiratory pressure (PEEP) ให้เหมาะสมสำหรับผู้ป่วยในขณะนั้นๆ ซึ่งจะทำให้ถุงลมที่แฟบอยู่เปิดออก ลดการกระชากเปิดปิดถุงลม เพิ่มประสิทธิภาพของถุงลมในการแลกเปลี่ยนก๊าซออกซิเจน ลด intrapulmonary shunt PEEP ที่เหมาะสมที่สุดคือ PEEP ที่ทำให้การแลกเปลี่ยนก๊าซออกซิเจนดีที่สุดและ compliance หรือความยืดหยุ่นของปอดเพิ่มขึ้นมากที่สุด.7
ในทางปฏิบัติ การหา PEEP ที่เหมาะสมทำได้ 2 แบบ คือ การค่อยๆ เพิ่ม PEEP ทีละน้อย แล้วหาจุดที่ทำให้ได้ compliance มากที่สุด SpO2 สูงสุดกับการเพิ่ม PEEP ให้สูงสุด แล้วค่อยๆ ลดระดับลง.
4. ไม่ควรตั้ง FiO2 สูงเกินไป นานๆ เพราะจะเกิด oxygen toxicity ทำลายเนื้อปอดได้ ถ้าเป็นไปได้ควรพยายามลด FiO2 ให้ได้ต่ำกว่า 0.6
สรุปแนวทางการตั้งเครื่องช่วยหายใจในผู้ป่วย ARDS แสดงไว้ในตารางที่ 1-2.

5. การใช้เครื่องช่วยหายใจแบบ high -frequency oscillator (HFO) นับเป็นอีกทางเลือกหนึ่งในผู้ป่วยเด็กที่เป็น ARDS10 ที่ไม่ดีขึ้นหลังจากใช้เครื่องช่วยหายใจแบบ conventional ดังที่กล่าวมาข้างต้นโดยเฉพาะผู้ป่วยที่มี air leak เช่น มี pulmonary interstitial emphysema, pneumo-thorax เป็นต้น.
2. ยา
ได้แก่ ยานอนหลับ, ยาลดความเจ็บปวด, ยาคลายกล้ามเนื้อ ควรใช้ด้วยความระมัดระวัง เมื่อมีข้อบ่งชี้ที่ชัดเจน ยาอื่นๆ เช่น activated protein C, steroid, nitric oxide, surfactant ยังอยู่ในระหว่างการวิจัย ยังไม่แนะนำให้ใช้เนื่องจากยังมีข้อมูลไม่เพียงพอ.
3. การดูแลรักษาด้านโภชนาการ สารน้ำ และเกลือแร่
ถ้าไม่มีข้อห้าม ควรให้อาหารทางกระเพาะอาหารผ่าน nasogastric tube เพื่อให้ได้พลังงานที่พอเพียง ช่วงระหว่างที่ feed ต้องจัดท่าผู้ป่วยให้ศีรษะสูงขึ้น เพื่อลดความเสี่ยงต่อการสำลัก.
ไม่ควรให้สารน้ำมากเกินไป เพราะอาจทำให้มีการรั่วของสารน้ำเข้าไปถุงลมมากขึ้น จากการวิจัย ในต่างประเทศพบว่าการให้สารน้ำปริมาณน้อย ได้ผลลัพธ์ในการรักษาดีกว่าให้สารน้ำปริมาณมาก ทำให้ oxygen index ดีขึ้น. ผู้ป่วยสามารถหยุดการใช้เครื่องช่วยหายใจได้เร็วขึ้น ซึ่งสอดคล้องกับประสบการณ์ที่ PICU โรงพยาบาลรามาธิบดี. นอกจากนี้ ยังพบว่าในผู้ป่วยบางราย การให้ albumin ร่วมกับ furosemide จะทำให้ภาวะการแลกเปลี่ยนออกซิเจนและ hemodynamic ดีขึ้นด้วย.11
4. การรักษาและป้องกันปอดอักเสบแทรกซ้อน จากการใช้เครื่องช่วยหายใจ
โดยทั่วไปแพทย์มักจะให้ยาปฏิชีวนะแก่ผู้ป่วย ARDS เกือบทุกราย เนื่องจากผู้ป่วยอยู่ในภาวะวิกฤตไม่สามารถรอผลการตรวจทางปฏิบัติการ ที่สำคัญคือ มีอัตราเสี่ยงต่อการเสียชีวิตสูง โดยมัก จะเริ่มจากยาปฏิชีวนะที่สามารถครอบคลุมเชื้อที่มีโอกาสเป็นสาเหตุของ ARDS มากที่สุดไปก่อน.
แนวทางที่จะสามารถช่วยลดความเสี่ยงต่อการเกิดปอดอักเสบจากการใช้เครื่องช่วยหายใจ ซึ่งเป็นภาวะแทรกซ้อนที่สำคัญในผู้ป่วย ARDS ได้แก่ การใช้ยาปฏิชีวนะเฉพาะเท่าที่จำเป็น, การดูแลช่องปากให้สะอาด, การพยายาม wean ผู้ป่วยจากเครื่องช่วยหายใจเพื่อให้ระยะเวลาที่ผู้ป่วยต้องอยู่กับเครื่องช่วยหายใจสั้นที่สุด, ไม่ sedate ผู้ป่วยมากเกินไป, ไม่เปลี่ยน ventilator circuit ถี่หรือห่างเกินไป, การกำจัดน้ำที่กลั่นตัวอยู่ในท่อ circuit และการใช้ in-line suction.12
สรุป
ความก้าวหน้าทางวิชาการในปัจจุบันทำให้เรามีความเข้าใจภาวะ ARDS มากขึ้น การใช้เครื่องช่วยหายใจอย่างสุขุมรอบคอบไม่มากจนเกินไป โดยการใช้ lung protective strategy และ recruitment maneuver เป็นส่วนสำคัญที่สุดที่จะทำให้ผู้ป่วยมีโอกาสรอดชีวิตสูงขึ้น. การใช้เครื่องช่วยหายใจแบบ high frequency oscillator เป็นอีกทางเลือกหนึ่งที่มีประโยชน์ในผู้ป่วยเด็กที่เป็น ARDS การรักษาแบบประคับประคองอื่นๆ ได้แก่ การใช้ยา การให้สารอาหารให้เพียงพอกับความต้องการของร่างกายที่มีมากขึ้น การจำกัดสารน้ำ การรักษาสมดุลของเกลือแร่ ตลอดจนการรักษาและป้องกันปอดอักเสบแทรกซ้อนจากการใช้เครื่องช่วยหายใจ เป็นส่วนที่จะสนับสนุนให้ ผู้ป่วยรอดชีวิตจากภาวะ ARDS อันน่าสะพรึงกลัวนี้.
เอกสารอ้างอิง
1. Bernard GR, Artigas A, Brigham KL, et al, and the Consensus Committee. The American- European consensus conference on ARDS : Definitions, mechanisms, relevant outcomes, and clinical trial coordination. Am J Respir Crit Care Med 1994; 149:818-24.
2. Martin TR. Cytokines and the acute respiratory distress syndrome (ARDS) : a question of balance. Nat Med 1997; 3:272-3.
3. Amato MB, Barbas CS, Medeiros DM, et al. Effect of a protective-ventilation strategy on mortality in the acute respiratory distress syndrome. N Engl J Med 1998; 338:347-54.
4. Gattinoni L, Caironi P, Cressoni M, et al. Lung recruitment in patients with the acute respiratory distress syndrome. N Engl J Med 2006; 354:1775-86.
5. Stewart TE, Meade MO, Cook DJ, et al, and the Pressure-and Volume-Limited Ventilation Strategy Group. Evaluation of a ventilation strategy to prevent barotraumas in patients with high risk for acute respiratory distress syndrome. N Engl J Med 1998; 338:355-61.
6. Acute Respiratory Distress Syndrome Network. Ventilation with lower tidal volume for acute lung injury and the acute respiratory distress syndrome. N Engl J Med 2000; 342:1301-8.
7. Suter PM, Fairley B, Isemberg MD. Optimum and end-expiratory airway pressure in patients with acute pulmonary failure. N Engl J Med 1975; 292:284-9.
8. Mancini M, Zavala E, Mancebo J, et al. Mechanisms of pulmonary gas exchange improve- ment during a protective ventilatory strategy in acute respiratory distress syndrome. Am J Respir Crit Care Med 2001; 164:1448.
9. Kacmarek RM, Dimas S, Mack CW, editors. The essentials of respiratory care. 4th ed. Missouri: Elsevier Mosby, 2005.
10. Arnold JH, Anas NG, Luckett D, et al. High frequency oscillatory ventilation in pediatric respiratory failure: a multicenter experience. Crit Care Med 2000; 28:3913-9.
11. Martin GS, Mangialardi RJ, Wheeler AP, et al. Albumin and furosemide therapy in hypo-proteinemic patients with acute lung injury. Crit Care Med 2002; 30:2175.
12. Kollef MH. Prevention of hospital-associated pneumonia and ventilator-associated pneumonia. Crit Care Med 2004; 32:1396.
อรุณวรรณ พฤทธิพันธุ์ พ.บ., ศาสตราจารย์
หัวหน้าหน่วยโรคระบบหายใจเด็ก ภาควิชากุมารเวชศาสตร์
คณะแพทยศาสตร์โรงพยาบาลรามาธิบดี
มหาวิทยาลัยมหิดล
- อ่าน 159,801 ครั้ง
 พิมพ์หน้านี้
พิมพ์หน้านี้




